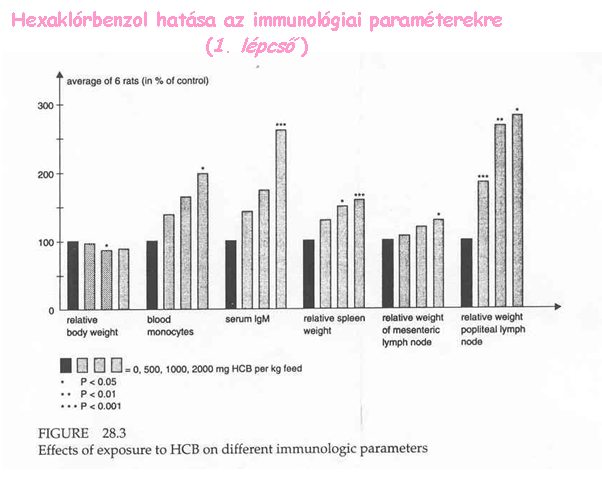
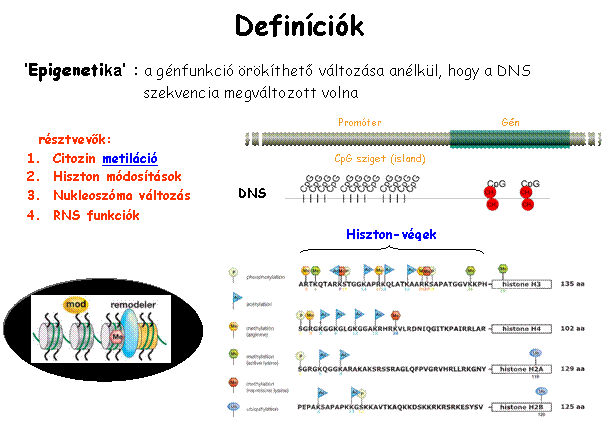
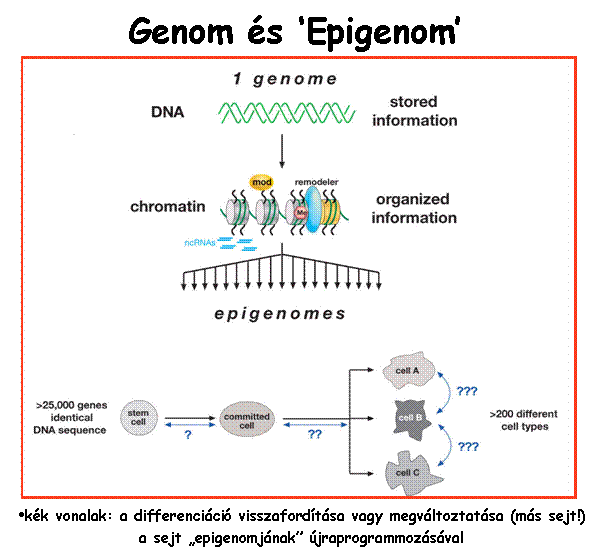
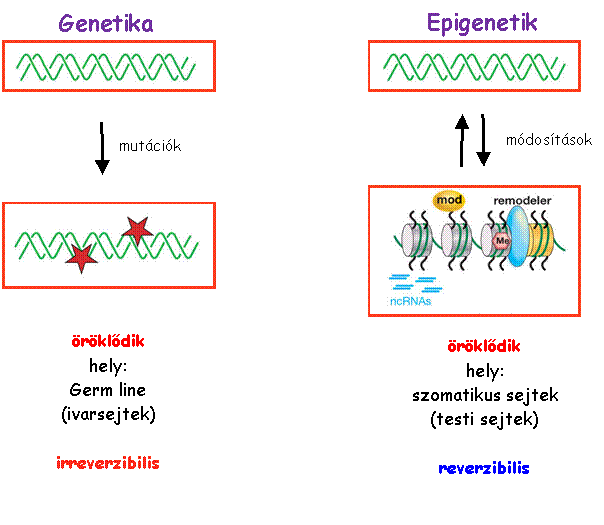
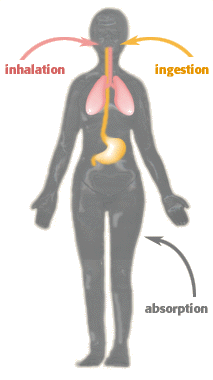'Egészségkárosító'.. Vizsgakérdések
2009.
1. (szervetlen és szerves)
környezetszennyező vegyi anyagok, eredetük, hatásuk a
környezetre és az egészségre,
összefüggés
szennyezés forrása:
- "természetes" - természeti
(nem-ember-okozta: vulkánok, vízalatti betörések)
- "antropogén" - ember általi
- ipar (nem megfeleően
tisztított szennyvíz – ld. Rába, 2007:
bőrgyár AT, baleset, olajok)
- mezőgazdaság
- bányászat
-
közlekedés/szállítás
szennyezők:
szervetlen
anyagok
(nehézfémek, szervetlen sók, nemfém-oxidok)
NITRÁTOK
Ø
természetes,
"hasznos" N-körforgás
Ø
EPA standard:
Nitrát-tartalom kevesebb lehet, mint 10 mg/L vízben, 2 mg/kg
talajban
Ø
magas
nitrát-koncentráció hipoxiát okoz (pl. "kék-baba
szindróma"), mérgező a melegvérű
élőlényekre (=toxikus)
Ø
Felszíni vizek
természetes nitrát-tartalma <1mg/L
Ø
Esszenciális
táplálék mind a növényeknek mind pedig az
állatoknak
Ø
Eredete: a
légkörből (pl. kipufogógáz),
műtrágya és természetes trágyák,
állati ürülék, szennyvíz, növényi
hulladék
Ø Víztisztító
művek nitráttartalma elérheti a 30mg/L-t
FOSZFÁTOK
Ø
A foszfor esszenciális
táplálék mind a növényeknek mind pedig az
állatoknak, a vízi tápláléklánc
fontos eleme
Ø
A foszfor a természetben
alacsony koncentrációban van és sokszor
korlátozottan áll az élővilág
rendelkezésére
Ø
Már
kismértékű poszfor-koncentráció
növekedés is indukálhat nagymennyiségű
növényi szaporodást, vízben pedig
algavirágzást - ezzel csökkenti a vízben oldott
oxigén mennyiségét ami halak és más
vízi állatok pusztulását vonja maga után
Ø
Eredete: talaj és
kőzetek, hulladékvíz, szennyvíz-kezelés,
műtrágyázás, állattenyésztés,
kereskedelmi tisztítószerek
pH
Ø
a pH a legtöbb kémiai
és biológiai folyamatra hatással van
Ø
a legtöbb
élőlény a 6.5-8.0 tartományt tűri. Magasabb vagy
alacsonyabb pH a biodiverzitást és a reprodukciós
képességet csökkenti
Ø
pH változások a 'savas eső' következtében fordulnak
elő
CO2
Ø
a vizek pH-ját
csökkenti (CO2 + H2O -> HCO3-
+ H+)
Ø a
mészkövet és dolomitot oldja - eróziót okoz
(CaCO3(s) +
CO2 + H2O -> Ca++ + 2HCO3-
+ 2H+)
Ø savasodást okoz
Ø melegház-hatású
gáz - az atmoszférában
szerves
anyagok
általában biológiai eredet . . .
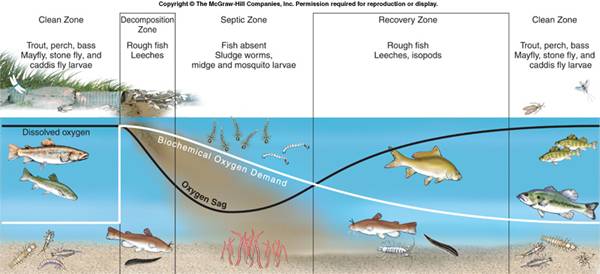
EUTROFIZÁCIÓt
okoznak
magas szervesanyag szint túl sok tápanyag: N>3ppm P>.01ppm
az
autotrof élőlények gyors növekedését
okozza (nagy algaszaporodás)
a
vízi növények pusztulása = fényhiány
a
vízi növények lebomlása –
oxigénelhasználódás, az oxigént
igénylő vizi élőlények pusztulása
“halálzónák
kialakulása”
Hipoxiás
környezet - <2.0mg/l oldott oxigén
Anoxiás
környezet – 0.0mg/l oldott oxigén
halaknak
4-5 mg O2/liter víz szükséges, tüdős
víziélőlényeknek kevesebb
|
|
|
|
|
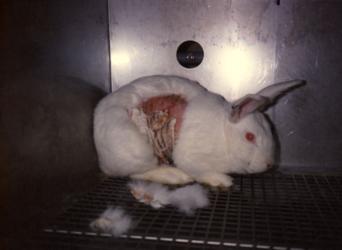
tengeri állatok pusztulása
vízszennyezést követően |
|
|
|
|
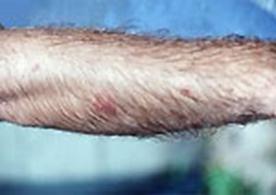
algatoxin hatása a
fürdőzőre (fekélyes gyulladások) |
algatoxin hatása a vizek
élővilágára (elpusztult halak) |
toxikus vegyi anyagok követik
a víz és a C-N-P körforgását
(oldhatóság, vízgőzdesztilláció,
gáz - pára)
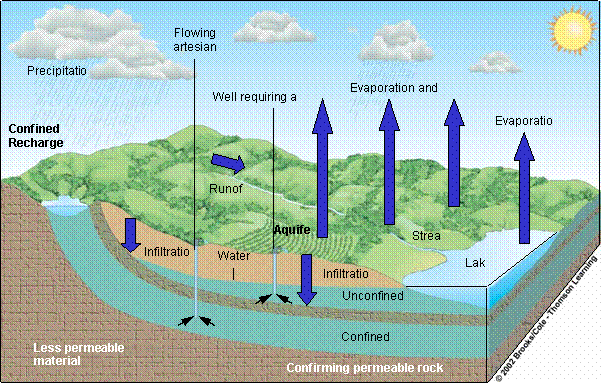
anyagok körforgása: a vízzel és a
légkörrel
|
|
szintetikus
termékek:
nehéz (lassú) biológiai lebomlás
peszticidek
2. A
méreg fogalma, mérgek EU besorolása,
expozíció, expozíciós utak, dózis fogalma,
bio-koncentráció, bio-akkumuláció
Paracelsus alkimista, orvos,
csillagász (1493-1541): Alle Ding sind Gift…allein
die Dosis macht, dass ein Ding kein Gift ist.
Minden
anyag méreg …egyedül a dózis határozza meg, hogy mi nem mérgező.
Méreg= mennyiségi, nem minőségi fogalom
vegyület,
amely a kísérleti állatok felét
elpusztító egyszeri adagja
(LD50) max. 50
mg/ttkg
Mérgek
besorolása az EU elvek (patkányokon meghatározott akut orális toxicitás) alapján:
|
1. Nagyon mérgező
(LD50<25mg/ttkg) pl.nikotin,
indometacin 2. Mérgező (LD50=25-200mg/ttkg) Pl.
aldrin (inszekticid) 3. Ártalmas
(LD50=200-2000 mg/ttkg) Pl.koffein 4. Méregkategóriába nem sorolható (LD50>2000mg/ttkg) Pl.konyhasó,
acetonitril (oldószer) Pl.
(patkány vizsgálat esetén): nem
méreg a konyhasó LD50=4000mg/ttkg méreg
a nikotin LD50=1mg/ttkg |
Dózis: A
szervezetbe jutott anyag
Akut
toxicitás: heveny toxicitás, egy anyagnak a
vizsgált szervezetben rövid idő alatt kifejtett
károsító hatása
Krónikus toxicitás:
idült toxicitás, egy anyagnak hosszú
időn át történő ismételt vagy folyamatos
bevitele esetén kifejtett károsító hatása
Kumulatív
toxicitás: egy vegyi
anyag tartós felhalmozódása a szervezetben (pl.
zsírszövetekben, csontokban)
Késői
toxicitás: a tünetek az
expozíciót követően
hónapok/évek/évtizedek múlva (esetleg a
következő generáció(k)ban) jelentkeznek
pl. daganatok, endokrin rendellenességek
Expozíció: az
a folyamat, melynek során a vegyi anyag meghatározott
környezeti feltételek mellett valamilyen módon kapcsolatba
kerül a szervezettel.
expozíciós
utak
|
|
•
orális (szájon
keresztül) – a vegyi anyagok evés vagy ivás
révén kerülnek a szervezetbe
•
inhalációs (belégzés) – a vegyi
anyagok belégzéssel kerülnek a tüdőbe
•
abszorpciós - a vegyi anyagok a bőrön
át kerünek a szervezetbe
|
A
bekerült vegyi anyag lehetséges sorsa a szervezetben: -
felszívódás -
eloszlás (függ az oldódási
viszonyoktól, szervek vérellátottságától) -
átalakulás (bomlás, enzimek szerepe) -
raktározódás (csont- és
zsírszövetekben) -
plazmafehérjékhez kötődés -
kiürülés (epével, verejtékkel,
vizelettel) |
Expozíció
– folyt
•
Expozíciós frekvencia –
“milyen gyakran”
•
Expozíciós időtartam –
“meddig tartott”
•
Expozíciós koncentráció
– “mennyi anyag”
|
|
|
a toxikológia a
tudományos eljárásokkal kapott eredményekre
épít
a
törvényszerűségeket/adatokat sok terület
használja
|
tud.
eredmények eredete |
toxikológiai
ismeret- felhasználók |
|
•
biológia •
kémia •
élettan •
orvostudomány •
gyógyszerészeti tudomány •
immunológia •
fizika •
statisztika •
környezettan |
•
törvényszéki orvostan •
klinikai kezelések •
gyógyszerfejlesztés •
közegészségügy •
ipari hygiene, munkaegészségügy •
állatorvostudomány •
mezőgazdaság •
környezet-egészségügy |
kémiai
biztonság: KOCKÁZATmegállapítás,
-kezelés
|
|
|
növényvédőszerek
áruház polcain |
Ø
Bioakkumuláció: valamely anyag
felhalmozódása a szervezetben vagy a
‘tápláléklánc’ szintjein
- átjut a
vér/agy gáton és a placentán
- nagyon lassan
távozik a szervezetből
- ha pl. egy
halszeletben találjuk, nem távolítható el
öblítéssel, kivágással vagy
főzéssel
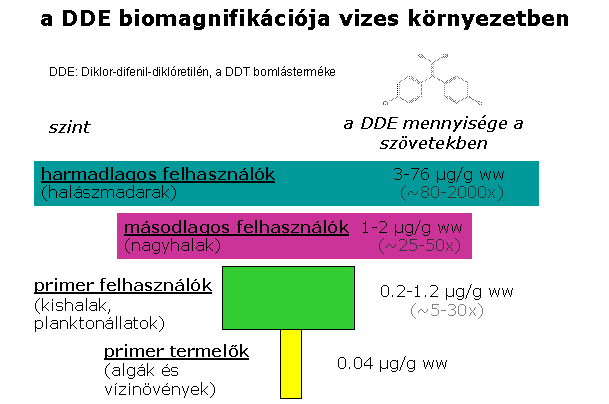
Ø
biokoncentráció
(biomagnifikáció): a tápláléklánc
felsőbb szintjein egyre magasabb akkumulált anyag
koncentráció mutatható ki
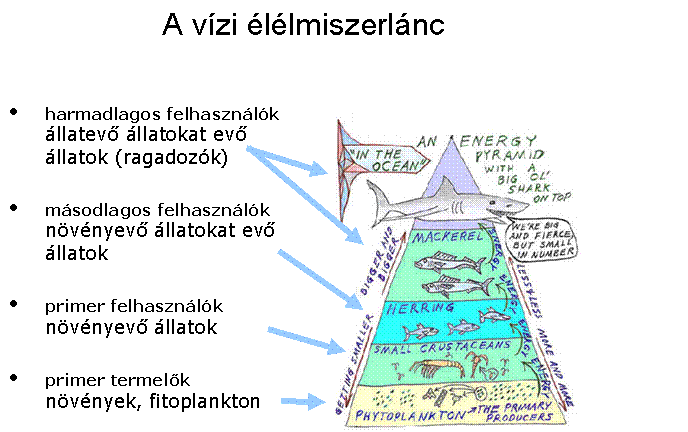
példa:
3. A veszélyes vegyi anyag fogalma, a
veszélyesség meghatározása, toxikológia,
dózis-hatás összefüggések

Ez a
veszélyesség meghatározása:
Veszélyesség: az
anyag szervezetbe jutásának és a mérgezés
bekövetkezésének valószínűsége

Toxikológia=toxicos+logos=méregtan
Toxikológia: méregtan; mérgek
és mérgezések tudománya, amely
-
mérgekkel
-
hatásmódjukkal
-
a
mérgezés tüneteivel, a mérgezettek
kezelésének lehetőségeivel
-
a
mérgek (törvényszéki) kimutatásával
foglalkozik
Toxicitás: mérgezőképesség (az
élő szervezetekre gyakorolt mérgező hatás.
Mértéke szerint okozhat átmeneti vagy tartós károsodást,
esetleg pusztulást
is)
befolyásoló
faktorok
•
külső
faktorok – a szervezeten/testen kívüli
tényezők
·
évszak
·
hőmérséklet
·
páratartalom
·
(nap)fény
•
belső faktorok
– a szervezetben
•
kor/érettség
•
genetkai
különbségek
•
testméret
•
Genus
•
Species
•
állattörzs
•
tenyészvonal
•
szex
•
élelem/ital
felvétel
•
fizikai
kondició
•
egészség/betegség
•
táplálkozási
hiányosságok
•
terhesség
•
szoptatás
Mérgező/toxikus: a szervezetbe kerülve egészségkárosodást
okoz
4. Akut és késői toxicitás fogalma,
példák
Akut
toxikus hatások
§
a tünetek gyorsan (azonnal –
órák múlva – napok múlva) jelentkeznek
§
azonnali ellátást igényel a
mérgezés
§
a tünetek a dózis
függvényében gyengék –
középerősök – erősek
(dózis-hatás összefüggés)
§
az expozíciót követően a
tünetek enyhülnek, megszűnnek
§
többnyire nem marad tünet a
túlélőkben (pl. HCN, gombamérgezés)
Késői
toxikus hatások
A krónikus
hatások sajátos formái:
n Hatásuk az
expozíció után csak hetekkel, hónapokkal, esetleg évekkel
(generációval?) később alakul ki
n Jellemző: az idő
előrehaladtával a tünetek fokozódhatnak
n A különböző
mechanizmussal kialakult tünetek hatása összeadódhat
(azaz az a hatások additívek, ill. szinergisták is
lehetnek)
A késői toxikus hatások típusai
n genetikai
állományra ható (genotoxikus), daganatkeltő (karcinogén)
n
utódokat károsító (teratogén)
n immunrendszert
károsító (immuntoxikus)
n idegrendszert
károsító (neurotoxikus)
n endokrin
rendszert befolyásoló („endokrin disruptor”)
Szerv-specificitás:
kardio-, nefro-, hepato-, neurotoxikus hatások
A késői toxikus hatások eredete
- környezeti
legjelentősebbek
a mezőgazdaságban használt vegyszerek
(herbicidek, peszticidek, inszekticidek, fungicidok,
műtrágyák, termésnövelők)
pl.: klorát
alapanyagú peszticidek felhasználói körében
daganatok, immunológiai eltérések gyakorisága
nő és nephritis, ill. akut vesekárosodás,
methemoglobinémia, hemoglobinuria és hemolízis is
gyakoribb
- munkahelyi
az
összes megbetegedések mintegy 4-8%-át jelentik
Magyarországon évente mintegy 1200-1400
új, munkahelyi
eredetű daganatos eset
genotoxikus hatások: a DNS szerkezetét
változtatják meg
5. Genotípus, fenotípus fogalma,
genotoxicitás, mutációk fajtái, szintjei
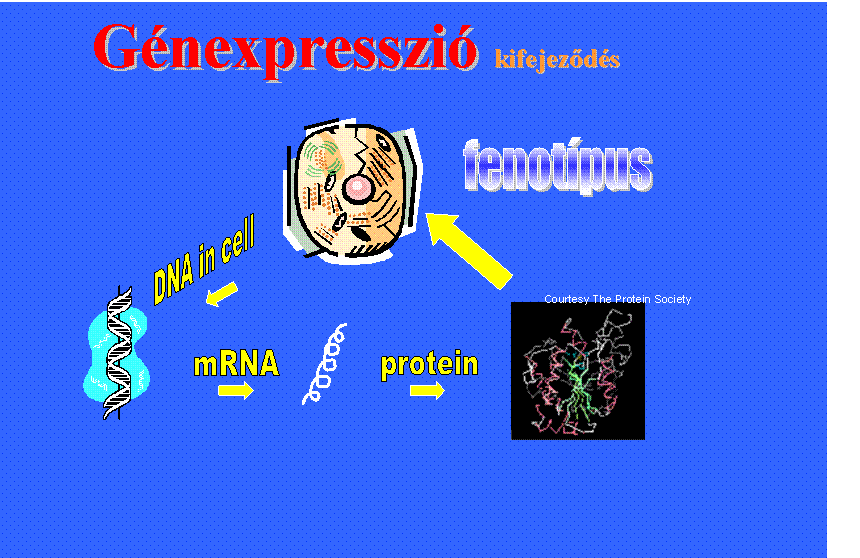
genotoxikus hatások: a DNS szerkezetét
változtatják meg
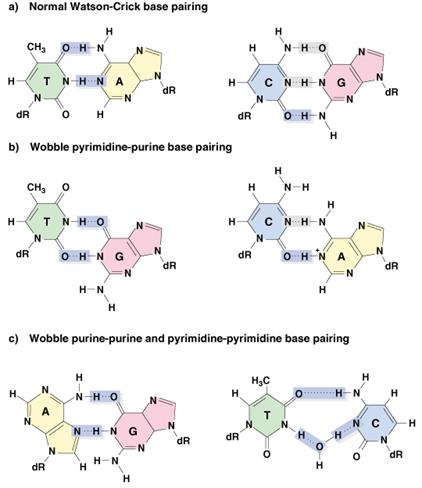
DNS
a sejt (élőlény) ÖSSZES tulajdonságát tároló
makromolekula, 109 építőegység
(bázispár), kétszálú szerkezet – komplementer
bázisok
a DNS
építőkövei: nukleotidok
nukleotid-párosodás
– a kettős spirál szerkezet alapja
a sejtben a DNS a kromoszómákban van
|
|
Humán kromoszómák n
hosszú DNS szálak (és protein) ~1,2 m
(!!) n
46 humán kromoszóma u
23 pár (homológ
parentális DNS) n
23-23 kromoszóma
öröklődik mindkét szülőtől |
|
Mutációk
a DNS szerkezetében
létrejövő eltérések
a mutáció szintjei
n
molekuláris szint (mutációk)
u nukleotid csere
(pontmutáció)
u nukleotid deléció
(törlés, kiesés)
u nukleotid inzerció
(behelyeződés)
n
kromoszóma szint (klasztogén
változások)
u szerkezeti változás
u kromoszóma számbeli
változás
Mutáns
n szokatlan, eltérő
fenotípus
n a mutációk
mutánsokat hoznak létre
|
|
|
pontmutációk eredménye:
- csendes
(„degenerált kód” – redundancia)
- aminosav
változás
(oldallánc-típus
– másodlagos fehérjeszerkezet -
funkcióváltozás)
helytől függő
hatás: (intergén régió / intron / exon /
szabályozó szekvencia)
leolvasási
keretelmozdulás („frame-shift”)
a fehérjetermék megváltozása: biológiai
aktivitás változás – fenotípus
változás
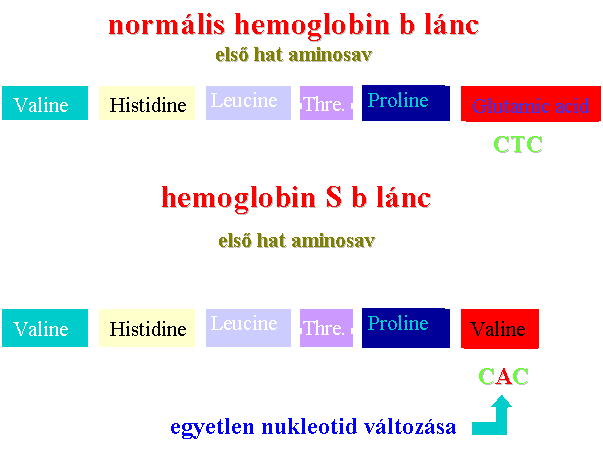
példa:
Génmutáció: akár
egyetlen báziscsere 'végzetes' lehet
|
|
|
|
|
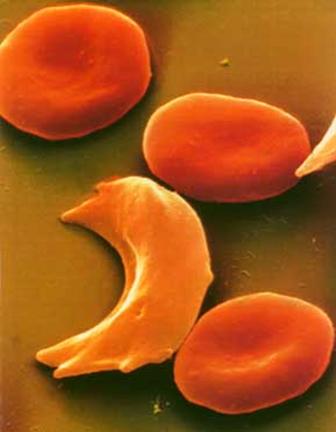
sarlósejtes
anémia (Sickle Cell
Anemia) a
hemoglobint kódoló gén megváltozott |
|
|
a mutációk okai
n Spontán - termodinamikai 'instabilitás'
u véletlenszerű
u kb. 1/100,000
a
génmutáció esélye
n
Indukált
u
mutagén
hatásokra
t sugárzások…DNS törések
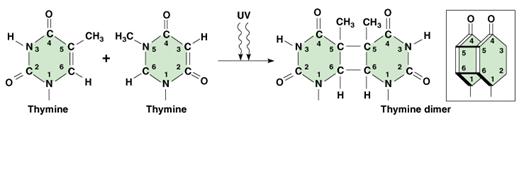
t UV
sugárzás….timin dimerek
t drogok…kromoszómatörések
t Cigarettafüst… kémiai anyagok ...
a daganatok
keletkezésének háttere:
mutagenezis
(DNS károsodások) vagy „kémiai karcinogenezis”
a mutációk típusai
n Germinális mutáció
u a meiózis során
keletkezik
u az embrió minden
sejtjét érinti
n Szomatikus mutáció
u a mitosis során keletkezik
u csak az érintett sejt utódsejtjeit
érinti
u rák - daganatok
példasor - nem kell felsorolni. . .
„Pontmutációs betegségek”
n Hemophilia
u véralvadási faktor
hiány
n Izomdisztrofia
u A dystrophin fehérje nem
termelődik
n Neurofibromatosis
u jelátadás rosszul
működik
n Aorta aneurizma
u Abnormális kollagén gyengíti az aortát
„kereteltolódási”
mutáció (frame-shift)
n egyetlen nukleotid
törlése (v. behelyezése) megváltoztatja a
fehérjekód értelmét
n példa: THE CAT ATE THE
RAT
az
első E törlése után:
THC ATA TET HER AT
---
értelmetlen „kód”
Abnormális LDL Receptor
|
|
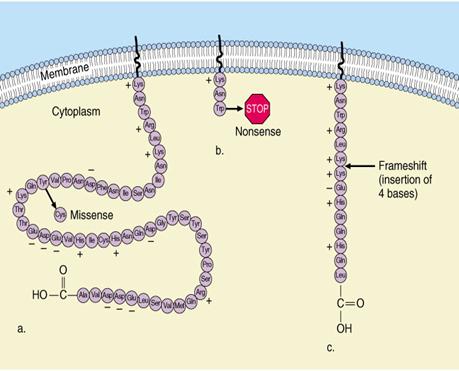
‘kereteltolódási’ mutáció rossz
fehérje keletkezéséhez vezet: funkciókiesés (STOP, v. csonka prot,
v. más aminosavak) a:
más aminosav b:
pontmutáció Arg CGA
STOP TGA c:
inzerció+kereteltolódás, |
kromoszóma-mutációk
ld. később
6. A
mutációk jelentősége, sorsa
Mekkora probléma??
körülbelül 1,000,000,000,000,000,000
(1018) DNS sérülés minden felnőtt emberben
naponta!
kb. 30.000.000.000 (3x1010) sejtünk
van . . . (~3x109/nap/sejt)
A LEGTÖBB MUTÁCIÓ SPONTÁN,
DE KÉMIAI ANYAGOKKAL (mutagének) INDUKÁLNI IS LEHET
MUTÁCIÓT –
nő a mutációs frekvencia
felsorolás - max egy kell
|
|
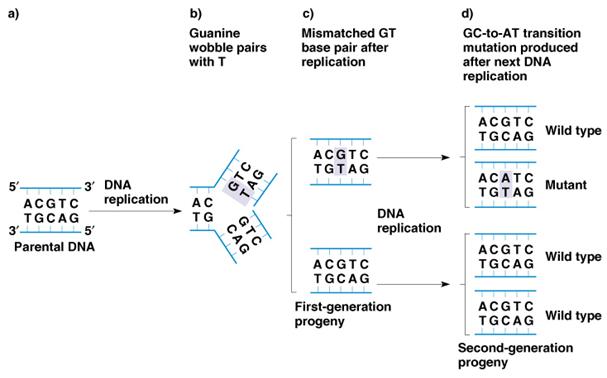
DNS szintézis
‘duplikáció’
pontos
kópia képződik –
hacsak nincs mutáció
magyarázat:
|
|
•
Mismatch
– helytelenül illesztett bázisok
–
Polimeráz
hiba, kb 1 hiba/104 bázis
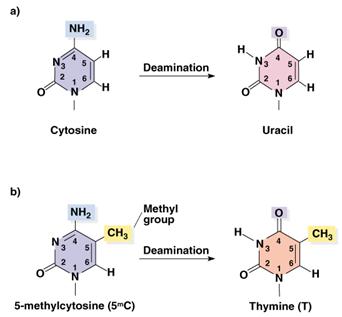
–
Dezaminálás
(C - U változás, C-G, U/T-A)
•
báziskiesés.
Purinvázas nukleotidok hidrolizálnak a
detoxiribózról: AP-hely
•
szerkezeti
sérülés. Dimer keletkezés.
•
foszfodiészter
kötések elhasadása – kémiai vagy
sugárzás hatására
max 4 kell
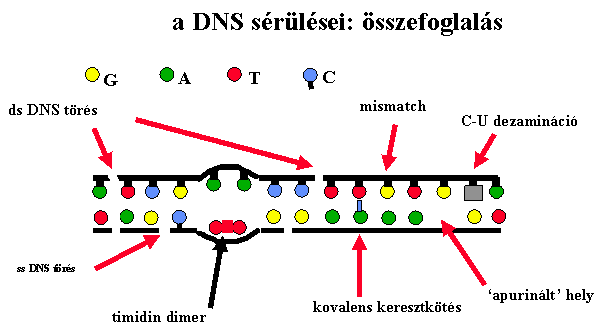
|
|
ds - duplaszál, ss - egyszál
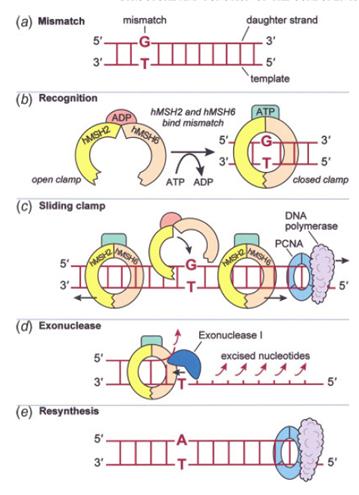
A hibákat (mutációkat) a sejt javítja !
DNS javító (repair) rendszer:
- rossz párosodás
- inzerció
vagy deléció az egyik
szálban
- DNS egyik vagy mindkét
szál (kromoszóma)-törések
REPAIR/JAVÍTÓ
MECHANIZMUSOK MŰKÖDÉSE: A
TÚLÉLÉS FELTÉTELE
|
|
magyarázat
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
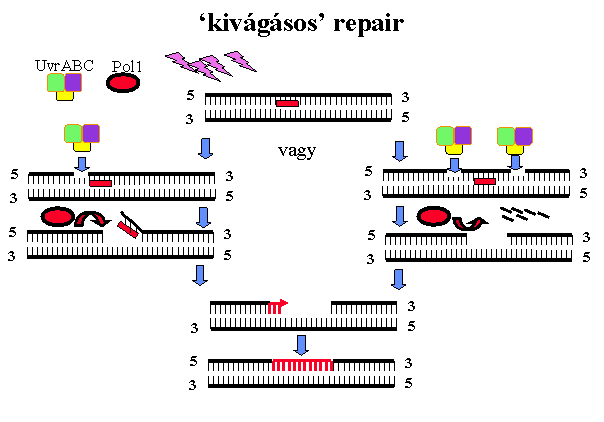
•
Excision/kivágásos
repair: 20 nukleotidig működik
•
uvrA,BC
(D) mutánsok
UV-érzékenyek
•
Mismatch
repair:
•
Az
excision repair egy formája.
Dam methylase is részt vesz
|
|
•
N-glikoziláz
kivágásos repair
•
Uracil
vagy helytelenül épül be vagy C dezaminálódik
U-lá
•
Uracil
N-glycosylase kétrehoz egy AP helyet
•
AP
endonukleáz felnyitja a szálat
•
javítás
történik mint a fenti ábrán
|
|
magyarázat vége . . . . . . . . . . . . . . . .
a
hibák eredete:
táplálék, táplálkozás
napfény,
UV-A, UV-B, ionizáló sugárzás, oxidatív
károsodás (javítása)
természetes és mesterséges környezet: vegyi anyagok
a DNS természetes metabolizmusa (minden sejt minden nap kb. 20,000 bázist veszít a
DNS-éből)
timin-dimerek
képződése
|
|
A hibákat (mutációkat) a sejt javítja !
DNS javító (repair) rendszer:
- rossz párosodás
- inzerció
vagy deléció az egyik
szálban
- DNS egyik vagy mindkét
szál (kromoszóma)-törések
mi
történik, ha a DNS repair hibás/hiányzik ?
súlyos
betegségek, több rák-hajlamosító hatás
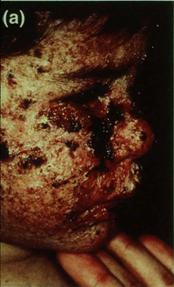
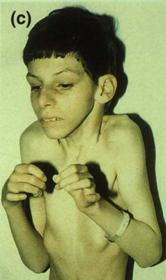
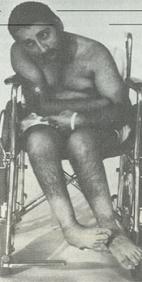
ne magold be!
pl:
Ataxia
telangiectasia (AT)
Cockayne
syndrome
Hereditary
non polyposis colon cancer (HNPCC)
Trichothiodystrophy
(kénhiányos
haj, hámlás-zavar)
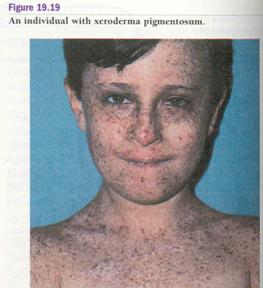
Xeroderma
pigmentosum (XP)
Bloom’s
syndrome
Fanconi
Anaemia
Nijmegen
Breakage Syndrome
Werner
syndrome
(nagyon ritka
betegségek)
|
XP |
XP |
Cockayne
syndrome |
AT |
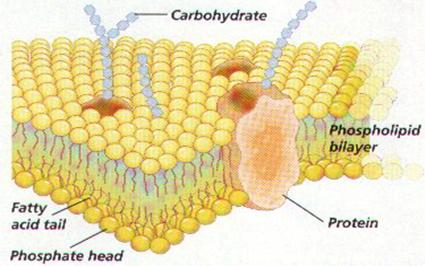
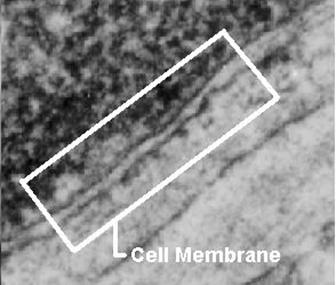
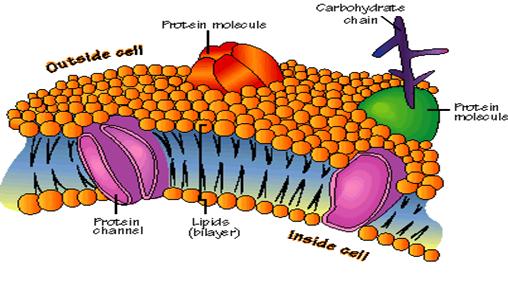
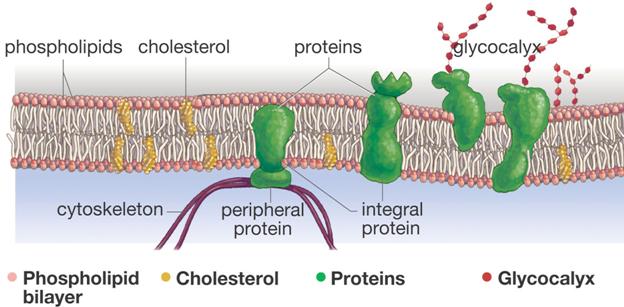
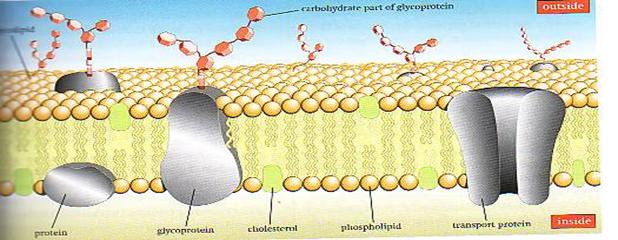
7. Plazmamembrán: szerkezet, összetétel
|
|
|
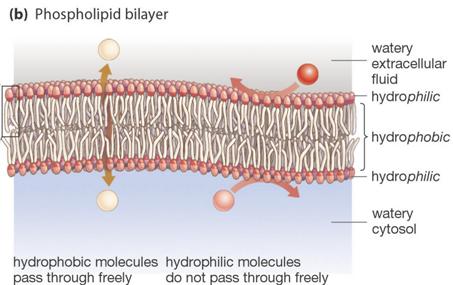
foszfolipid kettős réteg (koleszterin!)
– hidrofil/hidrofób
fehérjék
szénhidrárok
tér-elválasztás:
extracelluláris tér – intracelluláris tér
(citoszol)
védő
határ(oló)
’a sejt kapuja’
– minden anyagforgalom a plazmamembránon keresztül
történik
szelektív bemenő-kimenő
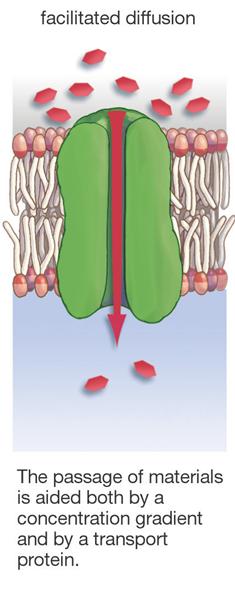
anyagforgalom: TRANSZPORT
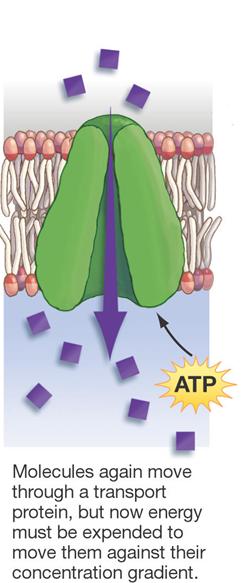
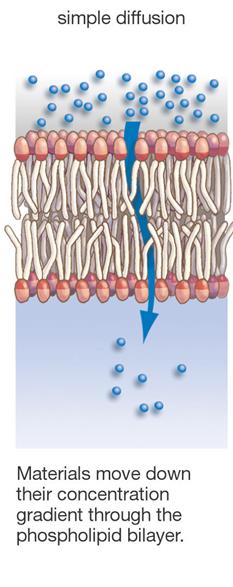
DIFFÚZIÓ – „FACILITÁLT
DIFFÚZIÓ” - AKTÍV
TRANSZPORT
flexibilis – a sejt mozog
(migráció)
külső (extracelluláris) tér információinak
felisemrése
sejt-sejt közötti kapcsolatok (mechanikus,
információs)
sejten belüli
„talaj” – rögzítő
funkciók
nagyon sok enzim a plazmamembránon/ban „ül”
|
|
|
|
a ’fluid-mozaik’
modell
|
|
fluid: az individuális
foszpholipidek és fehérjék a rétegben szabadon
mozoghatnak, mintha folyadékban úsznának
mozaik: szabadon
kialakulnak fehérje-mintázatok (fehérjecsoportok)
|
|
kis és nagyobb
hidrofób molekulák és a víz viszonylag szabadon
átjárják
pl. CO2, O2, szteroidok, hidrofób peszticidek, stb.
hidrofil molekulákkal
szemben határoló
pl. ionok, fehérjék – polipeptidek
|
|
|
passzív transzport |
aktív transzport |
|
|
|
|
|
|
|
|
|
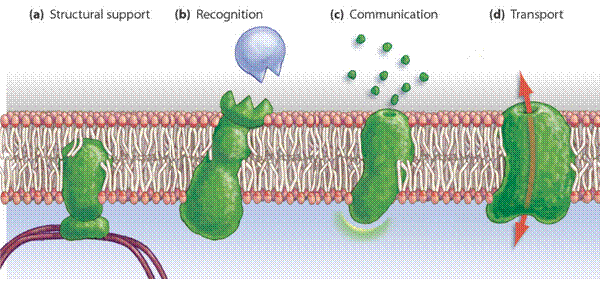
membránfehérjék:
|
|
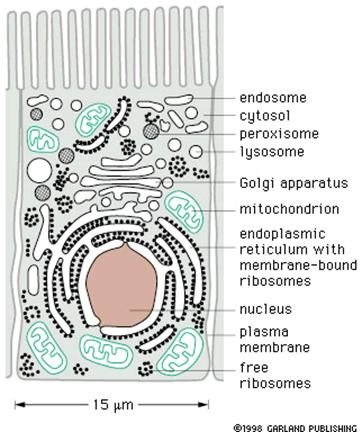
8. A sejt belső terei, ’kompartmentalizáció’
- funkciók
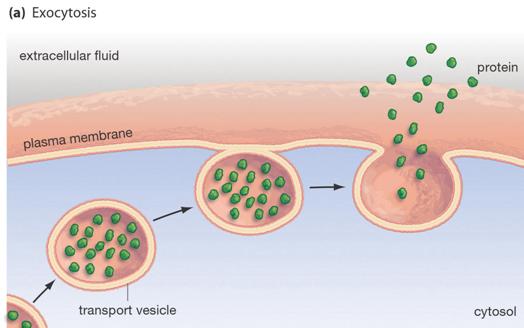
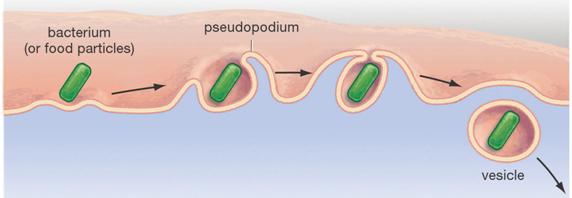
vezikulumok
nagy molekulák
kiűrítése: export / transzport vezikulumok
|
|
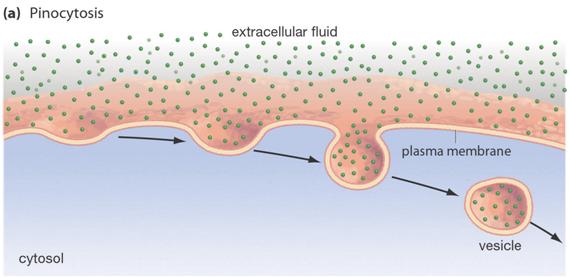
nagy (oldott v.
’szilárd’) molekulák felvétele: endocitózis
export / transzport vezikulumok
|
|
||
|
|
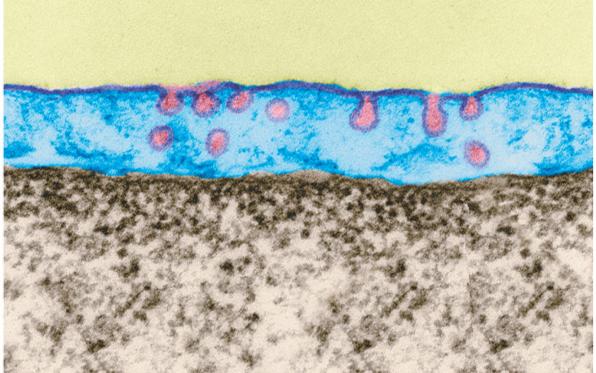
pl: kapilláris sejt
anyagfelvétele
|
|
|
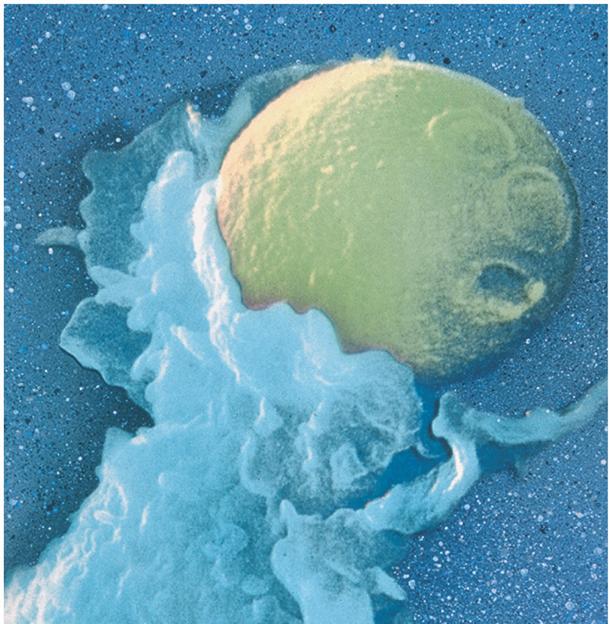
pl: immunsejt fagocitál
egy idegen testet
|
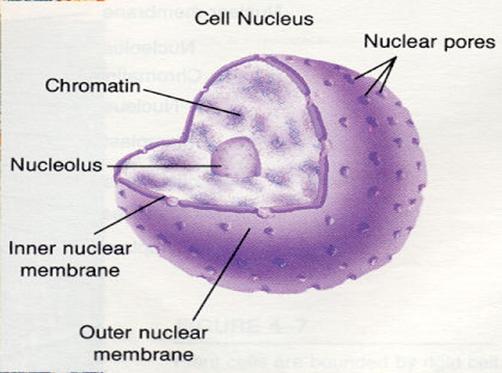
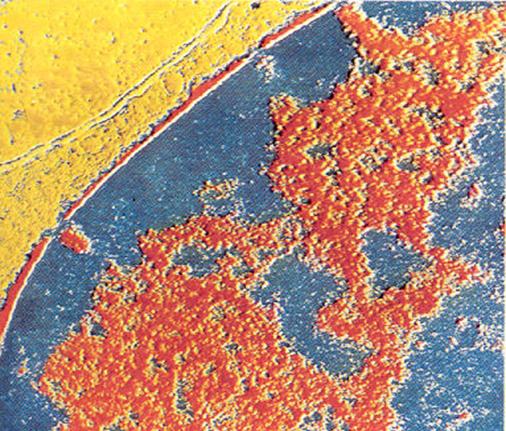
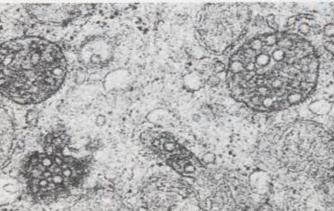
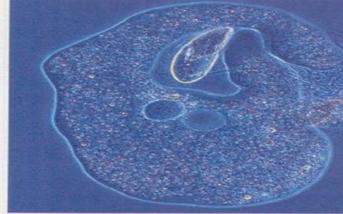
sejtmag, magmembrán
kettős membrán
pórusok (lyukak)
magvacska - transzkripció
|
|
a pórusok szerkezete EM képen
nagy molekulák transzportja
(ki és be)
|
|
mRNS – kifele
magfehérjék - befele
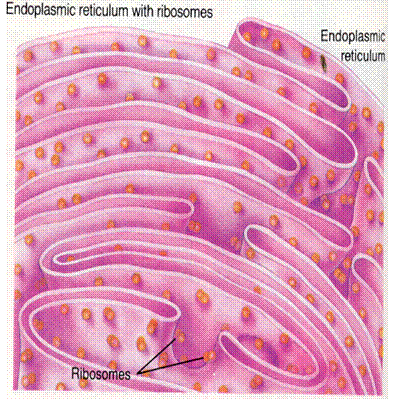
endoplazmatikus
retikulum (ER)
szemcsés és sima
összefüggenek
|
|
|
közvetlen
összeköttetésben a sejtmaggal
a kikerülő mRNS-ről
azonnal megindul a fehérjeszintézis
|
|
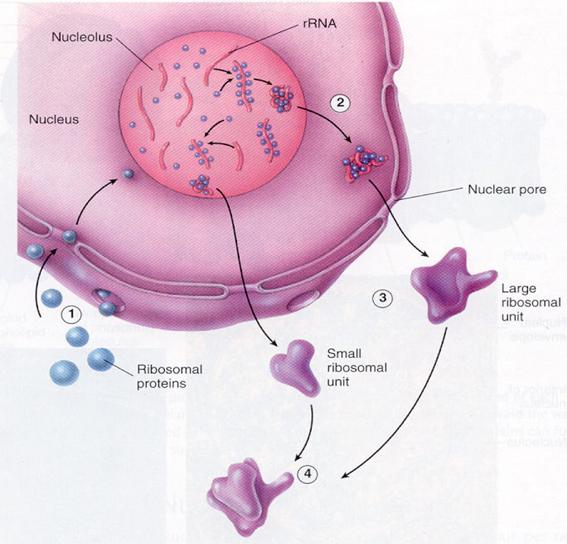
magyarázat:
1) három rRNS (28S, 18S, 2S)+
fehérjék
2) Riboszómális proteinek az
endoplazmatikus retikulumban készülnek és a sejtmagba
szállítják őket a transzporterek (nukleáris
póruson)
3) az rRNA a nukleoluszban
szintetizálódik és összeáll a megfelelő
riboszómális fehérjékkel: nagy és kis
riboszóma alegység
4) a nagy és kis
riboszóma-alegységek a pórusokon keresztül
elhagyják a sejtmagot
5) az alegységek kombinálódnak
és a riboszómákat hozzák létra –
kitapadnak az ER-hoz.
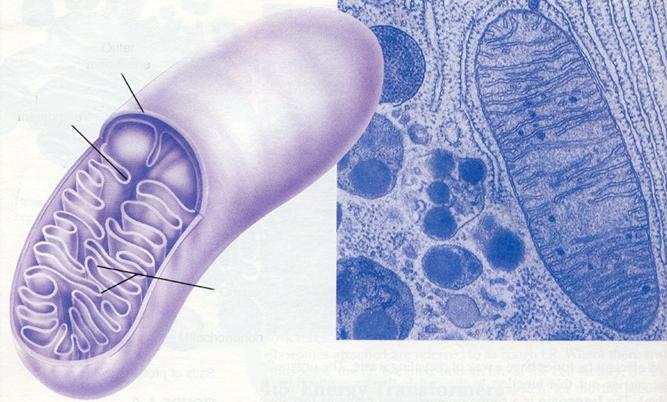
mitokondrium
nem
függenek össze más membrán-rendszerekkel (eml: 'szimbionta
bacik')
energiatermelés
táplálékmolekulákból:
sejtlégzés
C6H12O6
+ 6 O2 à 6 CO2 + 6 H2O + Energia
külső
membrán: hasonlít a
plazmamembránhoz
belső
membrán: sűrűn hajtogatott, kriszta
a
sejtlégzés a kriszták felületén
történik, enzimek
|
|
- saját DNS, RNS,
fehérjeszintézis
- a prokariota sejtekhez
hasonlít (kód, riboszóma)
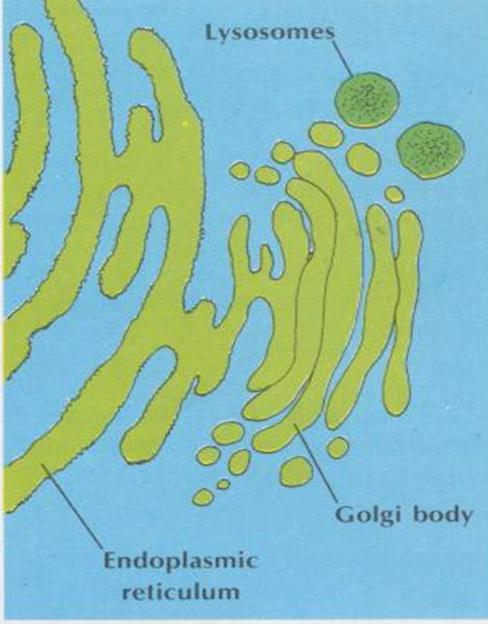
Golgi-apparátus
|
|
|
vezikulumok |
‘zacskók halmaza’
közel az ER-hoz
fehérjét tartalmazó zsákocskák az
ER-ból a Golgi komplexbe kerülnek
a Golgi csomagolja és szállítja a sejt által
termelt fehérjéket,
a fehérjemódosítások helye –
jelölés, szortírozás
apró vezikulumokban lefűződnek a Golgi zsákok
szélein
a Golgiban termelt és veziklumokba lefűzött
fehérjék vagy a sejt egy másik részére vagy
a sejtfelszínre kerülnek (szekréció)
pl. enzimek külső/belső felhasználásra,
hormonok, mérgek
lizoszóma
|
|
|
legöbölyödött
organellumok, emésztő enzimeket tartalmaznak
a Golgi
komplexből fűződnek le
emésztik
a felesleges vagy sérült sejtalkotókat,
táplálékrészecskéket, bekebelezett
vírusokat, baktériumokat
összeolvadnak
a plazmamembránnal és kiűrítik tartalmukat
(exocitózis).
a
sérült sejtalkotókat ismét
felhasználhatóvá teszi (aminosavak, oligopeptidek)
a sejtet a
lizoszóma-mambrán védi
az ER
Golgi és lizoszóma komplex
|
|
„kompartmentalizáció”
membránokkal
körülhatárolt terek, más és más
belső tartalommal, funkcióval, közeggel
|
|
9.
Fehérjék lebontási rendszere, útja
fehérjelebontás
– kikapcsolás
ubiquitin-rendszer (ub)
szerkezet
75 aminosav
konzervált (3 aa diff.
élesztő-humán)
|
|
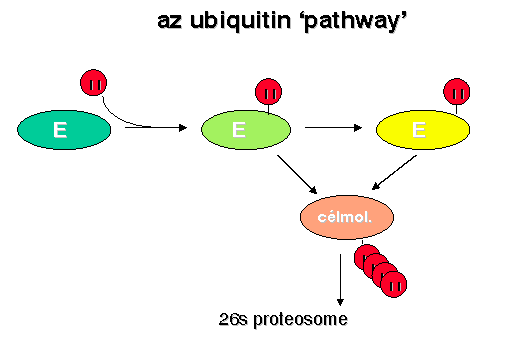
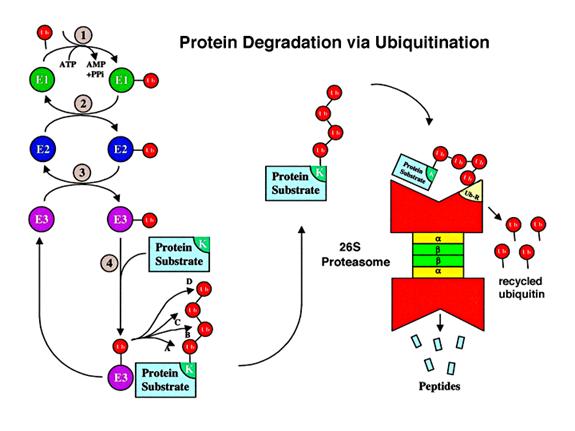
működés:
a lebontandó fehérjéhez sok ub
kötődik (poli-ubiquitinálás)
a 26S proteaszoma lebontja a fehérjét:
oligopeptidek
|
|
|
|
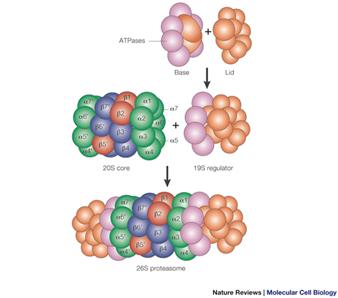
a
proteaszoma (proteasome)
|
|
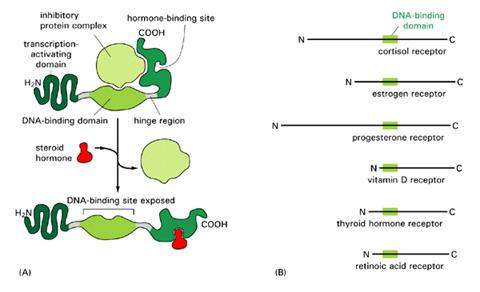
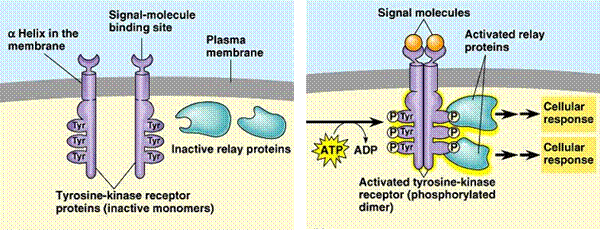
10. A sejt
jelátviteli rendszerei, membránhoz kötött és
intracelluláris receptorok
Signal transduction – jelátviteli
mechanizmus
a folyamat,
amely egy szignált követő sejtválaszt magában
foglalja
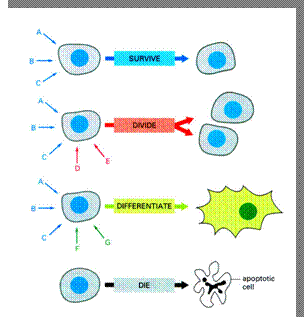
sejtválaszok
külső jelekre (szignálokra)
|
|
|
|
lehetséges
válaszok a szignálokra |
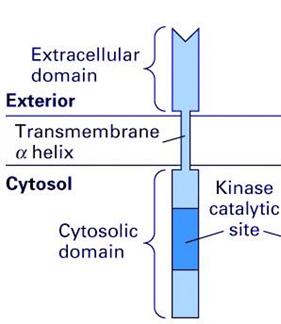
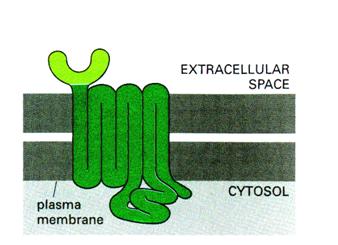
membránreceptor
felépítése |
|
|
sejtfelszíni
receptor: integráns
membránfehérje köt
a specifikus liganddal pl
polipeptid hormonok, növekedési faktorok intracelluláris
receptor: a
szignálmolekula a sejt belsejébe kerül és ott
aktiválja a sejtben v. sejtmagban lévő receptorát
pl. szteroidok, retinsav, tiroxin |
|
|
|
|
transzmembrán protein |
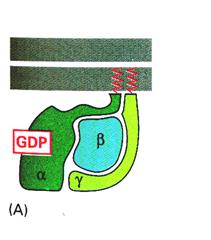
G-protein |
az intracelluláris
receptor szupercsalád
|
|
membránreceptoron át érkezik pl. az osztódási szignál
|
|
|
|
transzkripciós faktorok
aktiválása
osztódás-specifikus
gének átírása
sejtosztódás
indukciója
a sejtek
információs rendszere
11. Sejtciklus, sejtosztódás és
szabályozásának alapjai
A SEJTOSZTÓDÁS
modell:
sejtciklus
– a sejtek életcikusa
eredmény:
normális működés
növekedés/sejtpótlás
sejthalál
Sejtciklus
az a modell,
amely a sejt teljes életciklusát leírja,
egy sejtosztódás befejezésétől a
következő sejtosztódás befejezéséig
mese: nem
kellenek a nevek…
Howard és Pelc, 1954, Mitchison,
1972, Paul, 1982, Zetterberg 1986, Pardee, 1994
mitózis:
a két leánysejt keletkezése
– kromoszómák
egyenlően oszlanak meg
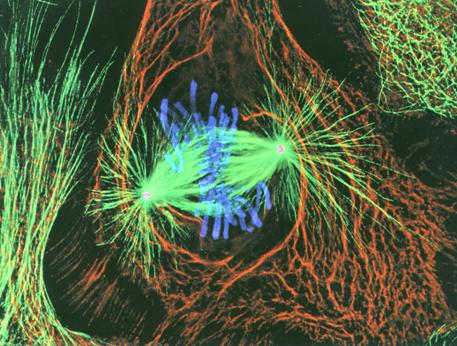
mitózis
|
centroszóma
- lila mikrotubulus -
zöld |
kromoszóma
– kék köztes
filamentumok - piros |
|
60xobj, 1250x |
|
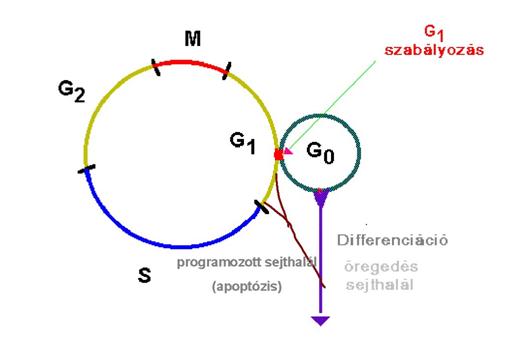
A sejtciklus fázisai, azok
időzítése gerinces (humán) sejtekben:
M: mitózis, a sejt két leánysejtet
képez osztódással. Időtartama 40-50 min
G1: 4
- 6 h a sejtosztódást
követő, a DNS szintézist megelőző
„nyugalmi” periódus
(„gap-1”)
G0:
0 h - akár több évtized. A sejt diffrenciált
működéseit végzi, a „terminális”
differenciáció kiinduló „helye”
S: 7,5
- 8 h DNS szintézis fázis (DNS duplikáció,
replikáció)
G2: ~2
h a DNS szintézist követő, a mitózist
megelőző „nyugalmi” periódus
(„gap-2”)
A sejtciklus szabályozási
lehetőségei
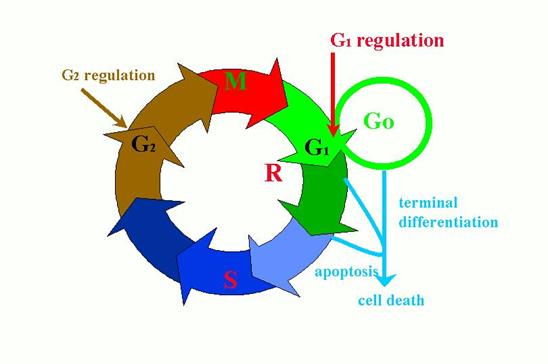
G1
szabályozás: a szabályozott sejtek normális testi sejtekre
jellemtő diploid kromoszómaállománnyal (DNS
mennyiséggel) rendelkeznek.
A daganatsejtek korai
formái is diploid sejtek.
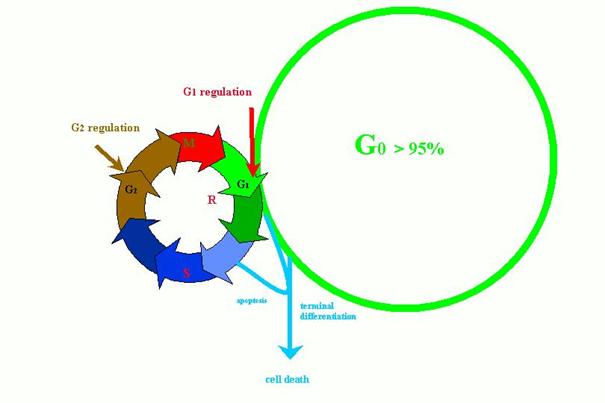
G2
szabályozás: nem jellemző a humán sejtekre
… a
valóságban a ciklusban és nyugalomban lévő sejtek
aránya < 5%:95%
körüli
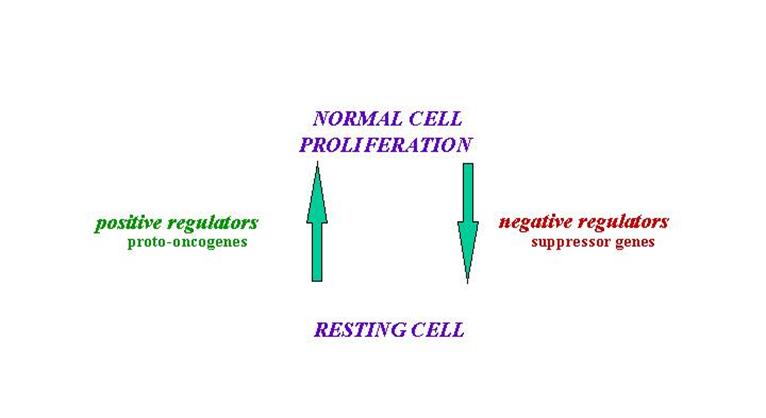
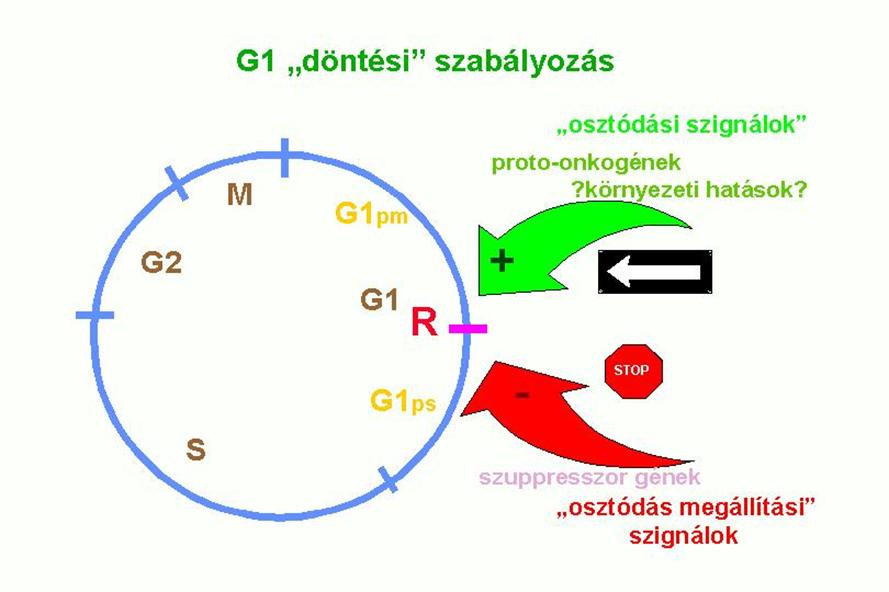
osztódás –
osztódási nyugalom: fenotípus
a fenotípust fehérjék alakítják
ki/határozzák meg
szabályozás: fehérjék
szintézise/degradációja/inaktiválása
fehérjeszintézis: transzkripció a génről
- transzkripciós faktor aktiválás
- szabályozó fehérje aktiválás
gyors
változás (néhány perc)
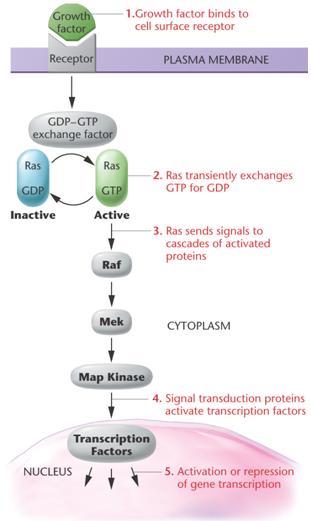
12.
Proto-onkogének, szuppresszor gének szerepe a
sejtosztódásban
a
mitotikus szignálátadási rendszer
![]()
![]()
![]()
![]()
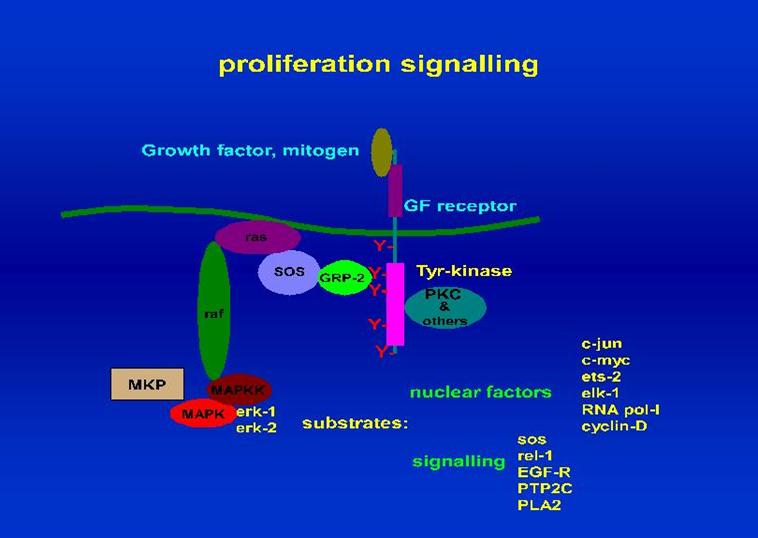
szabályozás: osztódj!? vagy NYUGI!!
mitotikus
homeosztázis
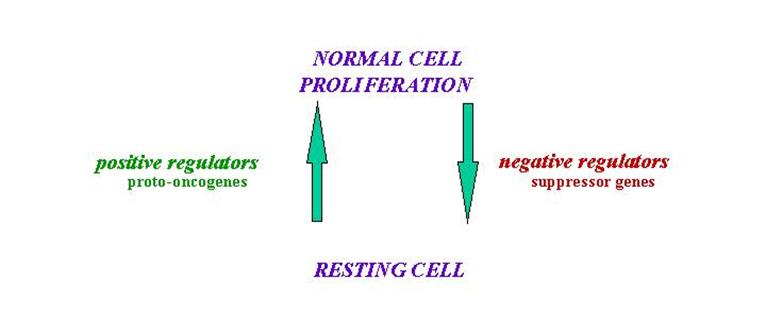
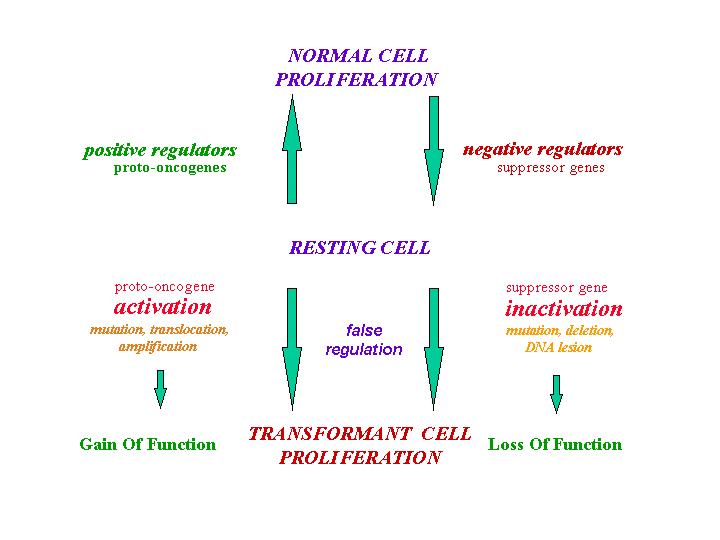
|
funkció
erősödés |
funció-vesztés/csökkenés |
molekuláris
hibák
daganatképződéshez
vezet(het)nek
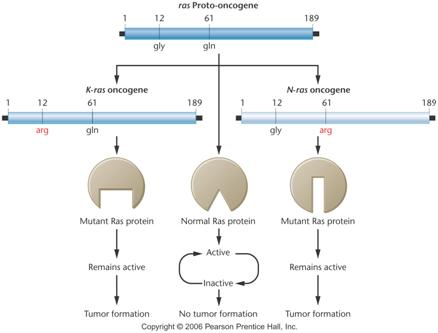
proto-onkogén
aktiváció
proto-onkogén
aktivációs mechanizmusok
mutáció
következménye: kóros (malignus) folyamat
pl.: ras
jelátvitel
|
|
|
. . – pontmutáció -
. . colorectális
karcinoma (vastagbél- végbélrák), gyomorrák,
(és ritkán: veserák, tüdőrák) |
|
|
szuppresszor
gén inaktiváció
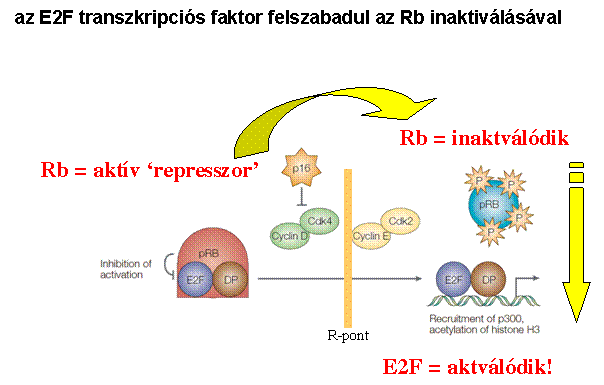
példa:
a 'retinoblasztóma gén' (Rb)
az E2F faktor nélkül a
sejt nem tud osztódni
az Rb
foszforilációja után már nem képes
megkötni az E2F-t
eredmény: E2F felszabadul
és megindul a sejt az osztódás felé
|
|
|
az RB
gén hibája esetén: nincs megállás a
sejtciklusban |
|
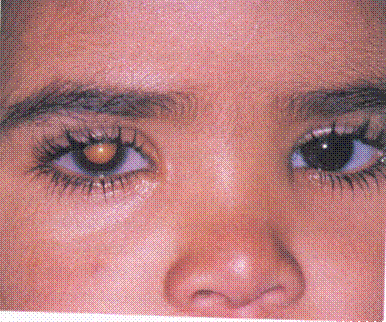
retinoblsztóma
–
sporadikus
- öröklött |
transzkripciós
faktorok
a
génátíráshoz (transzkripció) kellenek
|
NLS nukleáris
lokalizációs szignálpeptid DNS szekvencia-felismerő
domain DNS kötő peptid fehérje-kötő
(asszociációs) domain(ok) |
szuppresszor gén
inaktiváció következménye: nem lép a sejt a
nyugalmi (G0) fáisba hanem folyamatosan osztódik
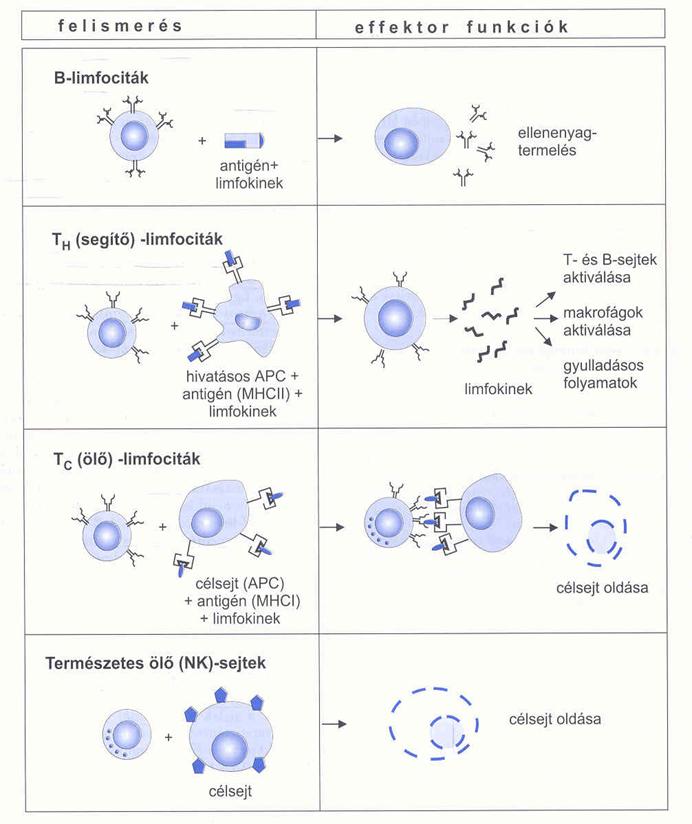
13. Milyen
limfocita populációkat ismer, és ezeknek milyen effektor
funkciójuk van?
|
|
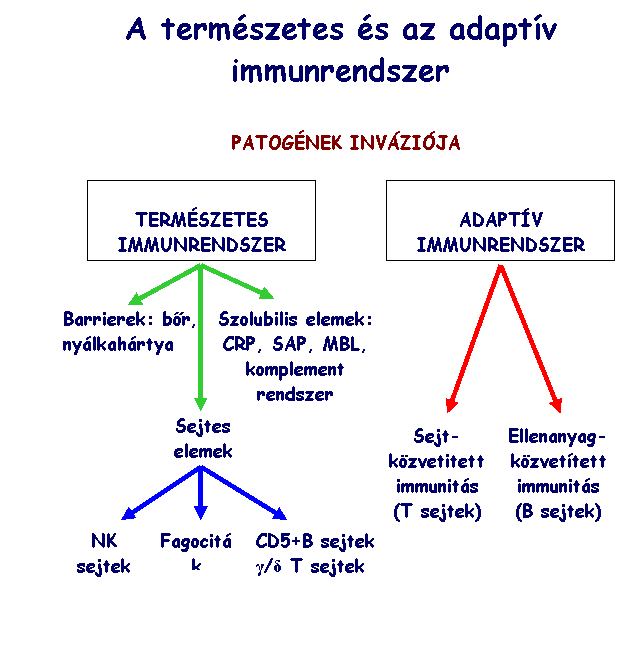
14. Mi
jellemzi a természetes és az adaptív immunrendszert?
|
|
|
|
azonnal reagál nincs memória |
lassan reagál
(1-2 hét) ’emlékszik’ legközelebb
gyors reakció |
nem választhatók szét
15.
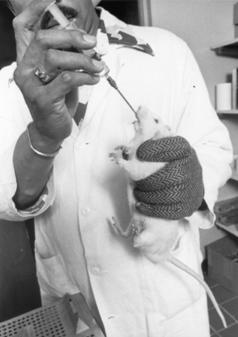
Jellemezze a laboratóriumi állatokon végzett
immuntoxicitási teszteket!
|
|
16. Az
immuntoxikus anyagok mely pontokon befolyásolhatják az immunrendszert,
és milyen választ válthatnak ki?
|
Az immuntoxikus
anyagok hatásai: Ølehetnek közvetlenül toxikusak Øsejtek pusztulása Øszövet degenerációja-
atrófia, fibrózis Øfunkciógátlás Øfokozott aktivitás (timusz, csontvelő) Økiválthatnak antigén-specifikus
választ Øtúlérzékenységi
reakciók Øgyulladásos folyamatok, szöveti
roncsolás (bármely szerv
érintett lehet: légzőszervek, bőr, emésztőrendszer,
urogenitális szervek, ízületek, központi
idegrendszer) |
17. Soroljon fel
három példát az endokrin rendszert
károsító anyagok (endokrin disruptorok) lehetséges
támadáspontjára
|
1.)
HORMONSZINTÉZIS Ø
Szintetizáló enzimaktivitás
módosulása Fenarimol (fungicid) aromatáz tesztoszteron −/_
ösztrogén Ø
Prekurzorok hiánya Kadmium koleszterin szintézis _
__ tersztoszteron _ Ø
Interferencia enzim kofaktorokkal Cu-kelátképzık
(ditiokarbamátok, szén-diszulfid) dopamin −/_
noradrenalin _
adrenalin 2.)
TÁROLÁS, FELSZABADULÁS Ø
amfetamin _ noradrenalin felszabadulás _ Ø
LH receptor agonisták _ Leydig sejtek tesztoszteron termelése _
hormonszekretáló
sejtek károsodása _ hiposzekréció 3.)
SZÁLLÍTÓFEHÉRJÉK A hormonok
fiziológiás hozzáférhetısége
függ: -totál -szabad
koncentrációjuktól Fehérjékhez
kötıdve: nincs receptorkötıdés Szállítófehérjék
hiány _ nem jut el a célszervekhez nagy mennyiség _
szabad
hozzáférés _ _
Néhány
xenoösztrogén _ szexhormon kötı globulin (TEBG) mennyiség _ _
Androgének,
glukokortikoidok _ TEBG _ _
Szalicilátok,
difenil-hidantoin _ tiroxinkötı globulin változása
_ szabad
tiroxin változása 4.) RECEPTOR-LIGAND
KÖLCSÖNHATÁSOK Az endokrin rendszert
károsító anyagok gyakran endogén hormonok szerkezeti
analógjai. AGONISTÁK Ø
Xenoösztrogének - metoxiklór - o,p'-DDT hidroximetabolitok - alkilfenolok - néhány PCB
metabolit - dietil-stilbösztrol ANTAGONISTÁK Ø
tamoxifen -antiösztrogén) Ø
vinclozolin (fungicid) metabolit -antiandrogén Ø
p,p'-DDE (DDT fı metabolit) -antiandrogén HORMONKÖTİ
RECEPTOR
TULAJDONSÁGAINAK MEGVÁLTOZÁSA Ø
TCDD Ø PCB ösztrogénreceptor
ösztrogén iránti érz. ê |
18. Az
endokrin rendszer felépítése, endokrin rendszer
működését befolyásoló anyagok
|
8.ea..\8-ea\EDhatas.htm. |
19. A női nemi
hormonok follikuláris szintézisében mi a szerepe a theca
és a granulosa sejteknek?
FZS 13. dia
20. Melyek az in
vitro reproduktív toxikológiai vizsgálatok főbb
típusai?
FZS 15. dia
21.
Karcinogén anyagok, hatások
karcinogén: daganatot
indukáló anyag/hatás
A karcinogének egy adott
populációban szignifikánsan emelik a daganatok
gyakoriságát
a karcinogén
1.
megváltoztatja a DNS-t
Mutagén
(genotoxikus)
daganatkeltő hatások:
a genetikai
állományban továbbörökíthető, a DNS
információtartalmát érintő
elváltozásokat, mutációkat okoznak
megvalósulás szintje: a sejtciklusban
funkció-aktiválás:
proto-onkogének
funkció-kiesés: szuppresszor gének
helytelen osztódás-szabályozás
a karcinogén
2. nem
változtatja meg a DNS-t
Nem mutagén (epigenetikus) daganatkeltő hatások:
modifikációk (azaz pl. a
fehérjék térszerkezetének
megváltoztatása) v. fehérjék expresszióváltozása
(DNS másodlagos módosítása) útján
hatnak
mindennapi példák:
(Cigaretta)füst
Sugárzások
Vegyi anyagok
Drogok
1. mutagén
karcinogének:
megváltoztatják a genotípust
· típusos mutagén
karcinogének az iniciátorok
· hatásuk sztochasztikus, küszöbdózisuk
nincs (!!)
· a mutagén karcinogének
MINDIG géntoxikusak
2. epigenetikus karcinogének:
megváltoztatják
a fenotípust
|
|
’működés’:
magyarázat. . .
|
|
a DNS metiláció megváltoztatja a
DNS metiláltságát (CG -> 5mCG,
palindrom!)
· génexpressziót
· fehérjeszintézist
· apoptotikus képességet
továbbá ezzel:
· sejtfelszíni receptorokat
· sejten belüli
jelátvitelt
· és pl. a
peroxiszóma proliferációt
tipikus epigenetikus karcinogének a daganat-promóterek
(kloroform, DDT, barbiturátok, hormonok)
hatásuk determinisztikus, van küszöbdózisuk
az epigenetikus karcinogének NEM géntoxikus
ágensek
megvalósulás szintje: a sejtciklusban
funkció-aktiválás:
proto-onkogének
funkció-kiesés: szuppresszor gének
helytelen osztódás-szabályozás
összefoglalva:
|
|
a
daganatképződés központjában nem-letális
genetikai hibák állnak
szabályozó
rendszerek
n
szuppresszor gének
sérülése/elvesztése
n
proto-onkogének aktivációja/amplifikációja
n
apoptózis gének sérülése/elvesztése
n
DNS repair gének sérülése/elvesztése
22.
Kémiai karcinogenezis mechanizmusa
Kémiai karcinogenezis
n direkt ható
karcinogének:
u alkilálószrek:
pl.: ciklofoszfamid
n indirekt ható
karcinogének:
prokarcinogének
az anyag metabolitja
karcinogén: aktváció szükséges (ultimate
carcinogen)
u Policiklikus szénhidrogének (PAH)
– pl.: benzpirán
u Aromás aminok, festékek
– pl.: benzidin
u Természetes anyagok:
pl.: aflatoxin
u Egyebek: pl.: vinil klorid, terpentin, stb.
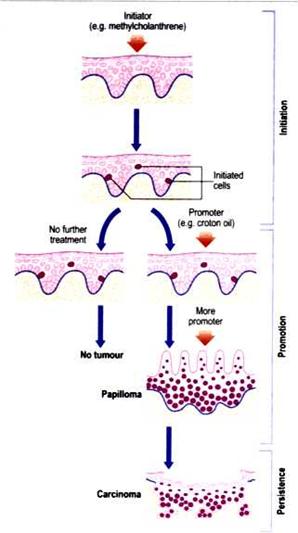
a kémiai karcinogenezis lépései
bélhám
|
|
Iniciáció DNS hiba (pl. penzpirán) -
egyszeri alkalommal is elég - Promóció Hisztologiai (szövettani)
változás
– (pl. terpentin - ko-karcinogén) -
éveken keresztül - Malignus transzformáció látható daganat –
további DNS hibák – néhány év! - |
A daganatkeltő hatás
kritériumai
Daganatkeltő: minden olyan ágens, ill.
hatás, amely:
n a kísérleti
állatokban, ill. az emberben daganatot okoz
vagy
n szignifikánsan emeli az adott populációban
létrejövő daganatok gyakoriságát
23.
Dózis, küszöbdózis, biztonsági
határértékek
dózis: analóg a koncentrációval, de
mégis más
egység: mennyiség/élő állat
testtömege – pl. mg/ttkg
játékpélda:
|
Ki kapta a
legnagyobb Tylenol dózist? acetaminophen –
fájdalomcsillapító |
|||
|
|
|
|
|
|
Testsúly: |
|
|
|
|
Tylenol: 300 mg |
600 mg |
100 mg |
50 mg |
a dózis
számítása:
|
|
||||
|
Tylenol: 300 mg |
600 mg |
100 mg |
50 mg |
|
|
Testsúly: 60
kg |
80 kg |
10 kg |
2,5 kg |
|
|
dózis mg/ttkg: 300/60=5 |
600/80=7,5 |
100/10=10 |
50/2,5=20 |
|
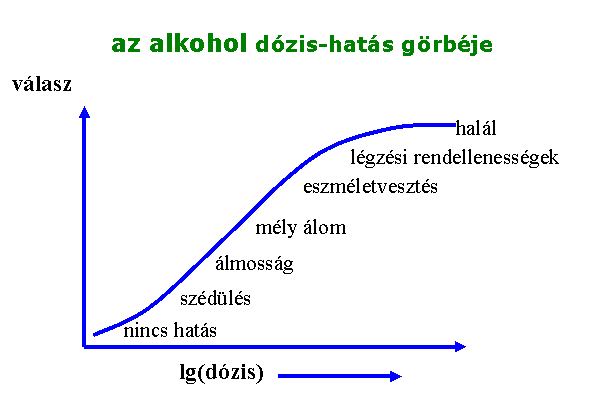
a biológiai hatás nem lineáris az alkalmazott dózissal
dózis-hatás
görbe
|
|
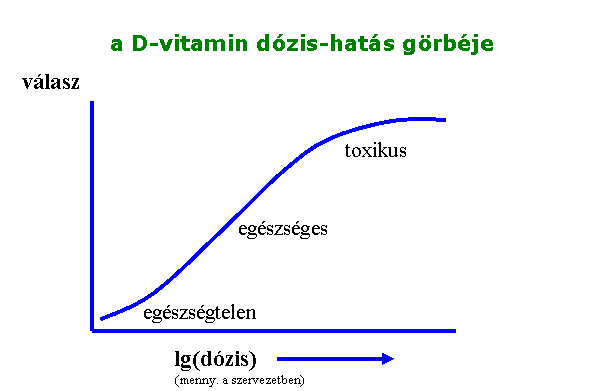
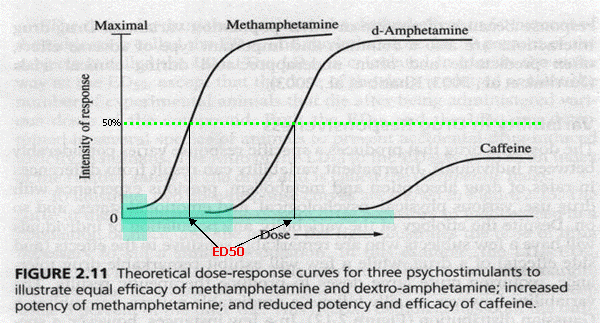
hathatóság és hatékonyság
|
|
fontos
értékek –
toxicitásra jellemzőek:
NOAEL – No Observable
Adverse Effect Level
nincs
kimutatható hatás („homeopátiás szint”)
LOAEL – Lowest Observable
Adverse Effect Level
már van biológiai hatás
|
ÁLTALÁNOS
KÜSZÖBÉRTÉKEK
|
24. A
kromoszóma mutációk típusai (pl.)
|
|
KoZsu diák: 10.ea. 19.dia
26. A
mikronukleusz képződése és kimutatása
KoZsu
diák: 10.ea. 29.dia
27. Az
Ames’ teszt Deák Vera anyaga
Deák
Veronika 10. ea. 13-20 ábrák
28.
Kockázat és kockázatkezelés fogalma,
stratégiái
kockázatok,
kezelésük
kockázatkezelés [risk management] ISO31000
a kockázat [risk]
azonosítása [identification]
felmérése (becslése) [assessment]
elsőbbségi sorrend
felállítása [prioritization]
a kockázat tényleges
megállapítása, előfordulásának
mérlegelése
a kockázatot
csökkentő tényezők felmérése,
értékelése
a
kockázatcsökkentés stratégiája
azonosítás:
eredet, probléma analízis
felmérés,
becslés [assessment]:
mennyiségi vizsgálatok –
laborvizsgálatok, analízis
előfordulás
gyakorisága v. valószínűsége
EU:
az OECD ajánlások (TEST GUIDELINES)
alapján
pl.
bőr irritáció
- OECD 404 / “Draize test”
|
|
szem
irritáció –
OECD 405
|
|
akut
toxicitás - OECD 402, 403, 420,
423, 425 (433, 434, 436)
|
|
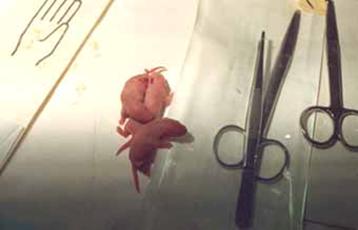
fejlődési toxicitás - OECD 414 (OECD
421/422) (900 nyúl, 1300 patkány)
|
|
karcinogenitás - OECD 451 + 453
|
|
“The Road to Replacement”
International
Perspectives & Opportunities for REACH
European
Coalition to End Animal Experiments
ECEAE.org
„alternatív
toxikológia” ICCVAM, ECVAM. JaCVAM – OECD
nem
kell tudni mindet: (főleg nem a számokat. . .)
|
•
Mutagenitás –
Ames/Bacterial Reverse Mutation
Test (OECD 471) –
In Vitro Chromosomal Aberration Test (OECD 473) –
In Vitro Cell Gene Mutation Test (OECD 476) –
In Vitro Sister Chromatid Exchange Test (OECD 479) –
In Vitro Micronucleus Test (draft OECD 487) •
Embryotoxicity (ECVAM-validated
Embryonic Stem Cell Test) •
Skin penetration rate (OECD
428 – in vitro skin absorption) •
Skin corrosion (OECD 431
– human skin model studies) •
Skin irritation (human clinical
skin-patch test – accepted in Canada/draft OECD Test Guideline) •
Eye irritation –
isolated bovine/chicken/rabbit
eyes, •
Phototoxicity (OECD 432
– 3T3 Neutral Red Uptake Phototoxicity Test) •
Pyrogenicity –
Limulus amoebocyte lysate (LAL)
test –
Endosafe© human blood
pyrogen test |
29. A
kémiai biztonság fogalma, alapvető elemei,
érvényességi köre, a szabályozás
általános alapelvei
31. Az
Európai Unió új vegyi anyag politikájának
alapelvei és alapelemei
Major Jenő 32-33-34-35
és 37-38 diák