kemkarc-multistep-diag-therapy
daganatkeletkezés
a genotoxicitás fogalma
a genetikai
állományra (DNS) ható
(genotoxikus) (késői) toxikus
hatások
a
hatás
többnyire daganatkeltő (karcinogén)
leggyakoribb alapja: a mutáció
a DNS szerkezetében
létrejövő eltérések
mutagén: mutációt indukáló anyag
pontmutációk eredménye:
- helytől függő hatás: (intergén régió / intron
/ exon / szabályozó szekvencia)
- csendes
(„degenerált
kód” – redundancia) - polimorfizmus
nincs élettani hatás
- aminosav
változás (oldallánc-típus – másodlagos fehérjeszerkezet - funkció)
- leolvasási keretelmozdulás („frame-shift”)
a protein termék megváltozása, biológiai aktivitás
változás
= fenotípus
változás
karcinogén: daganatot indukáló anyag
humán esetben - nincs kísérlet… -
a karcinogének az exponált
populációban szignifikánsan emelik adott daganatok gyakoriságát
a karcinogén
1.
megváltoztatja a DNS-t
Mutagén (genotoxikus) daganatkeltő hatások:
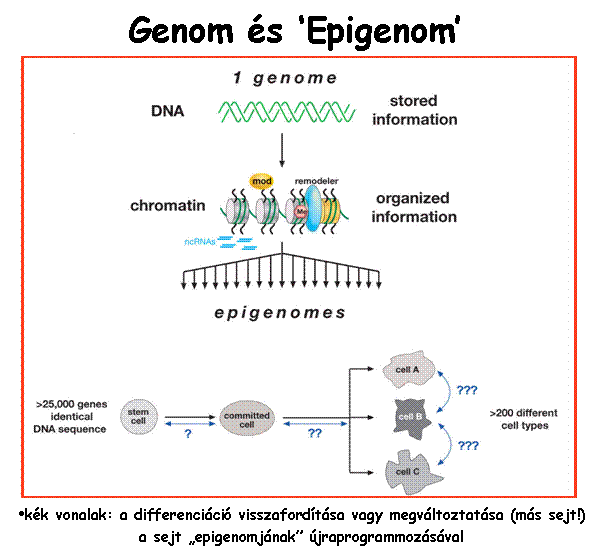
a genetikai állományban továbbörökíthető,
a DNS információtartalmát
érintő elváltozásokat, mutációkat okoznak
o
megvalósulás
szintje: a sejtciklusban
o
funkció-aktiválás:
proto-onkogének
o
funkció-kiesés:
szuppresszor gének
o
helytelen
osztódás-szabályozás
a karcinogén
2. nem
változtatja meg a DNS-t
Nem mutagén (epigenetikus) daganatkeltő hatások:
modifikációk (azaz pl. a fehérjék
térszerkezetének megváltoztatása) v. fehérjék expresszióváltozása (DNS
másodlagos módosítása) útján hatnak
mindennapi
példák:
(Cigaretta)füst
Sugárzások
Vegyi anyagok
Drogok
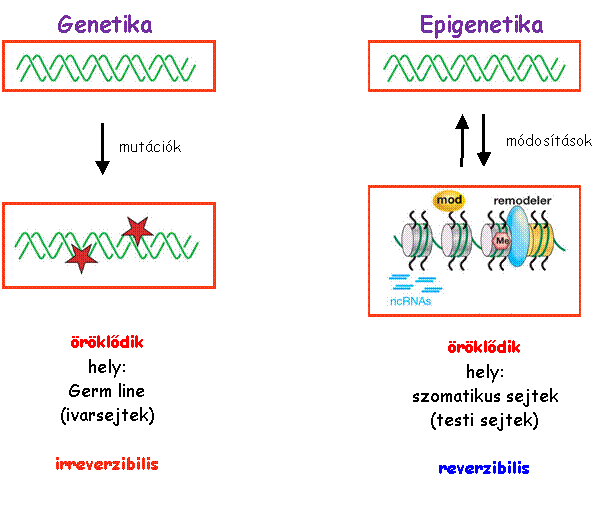
1. mutagén karcinogének:
(megváltoztatják a genotípust)
· típusos mutagén karcinogének az iniciátorok
· hatásuk sztochasztikus, küszöbdózisuk nincs (!!)
· a mutagén karcinogének MINDIG géntoxikusak
2. epigenetikus karcinogének:
megváltoztatják
a fenotípust
|
|
’működés’:
|
|
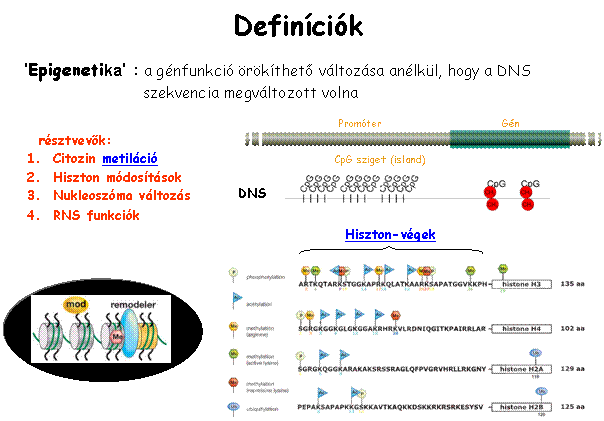
a DNS metiláció megváltoztatja a
DNS elérhetőségét (CG ->
5mCG, palindrom!)
· génexpressziót
· fehérjeszintézist
· gén szabályozást: pl. apoptotikus képességet
továbbá ezzel:
· sejtfelszíni receptorokat
· sejten belüli jelátvitelt
· és pl. a peroxiszóma proliferációt
tipikus epigenetikus karcinogének a promóterek
(kloroform, DDT, barbiturátok, hormon-szerű anyagok)
hatásuk determinisztikus, van
küszöbdózisuk
az epigenetikus karcinogének NEM géntoxikus ágensek
összefoglalva:
|
|
a daganatképződés
központjában nem-letális genetikai hibák állnak
meghibásodott
szabályozó rendszerek:
n
szuppresszor gének sérülése/elvesztése
n
proto-onkogének
aktivációja/amplifikációja
n
apoptózis gének sérülése/elvesztése
n
DNS repair gének sérülése/elvesztése
Kémiai karcinogenezis
(kísérletes
modellrendszerek)
n direkt ható
karcinogének:
u alkilálószrek: pl.:
ciklofoszfamid
n indirekt ható
karcinogének: prokarcinogének
az
anyag metabolitja karcinogén:
aktváció szükséges (ultimate carcinogen)
u Policiklikus szénhidrogének (PAH)
– pl.: benzpirán
u Aromás aminok, festékek – pl.: benzidin
u Természetes anyagok:
pl.: aflatoxin
u Egyebek: pl.: vinil klorid, terpentin, stb.
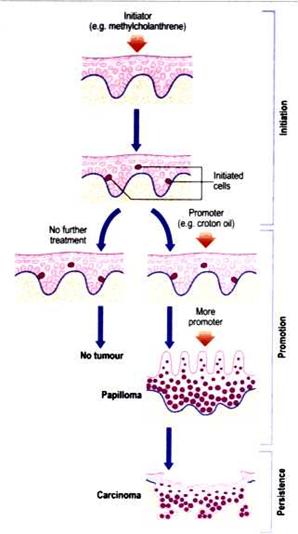
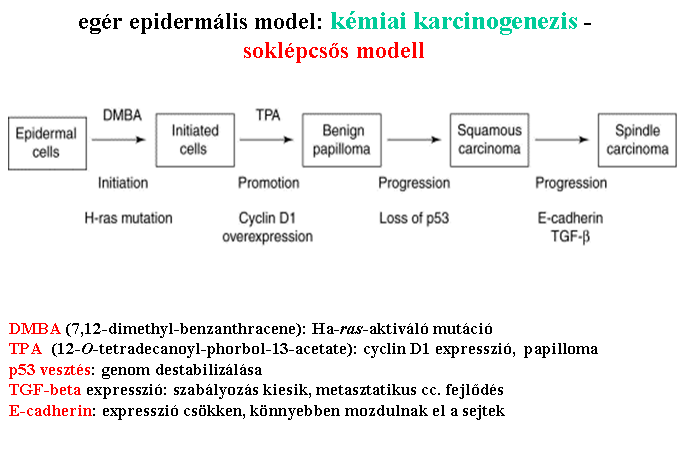
a kémiai
karcinogenezis lépései
bélhám
|
|
Iniciáció DNS hiba (pl. penzpirán) -
egyszeri alkalommal is elég - Promóció Hisztologiai (szövettani) változás – (pl. terpentin - ko-karcinogén) - éveken
keresztül - Malignus transzformáció látható daganat – további DNS hibák – néhány év! - |
A tapasztalat: a daganatok nem
'egyből', nem 'azonnal' alakulnak ki,
több
lépés, több változás/mutáció, hosszú idő szükséges (2-30 év)
iniciális mechanizmus
-
proto-onkogén aktiváció
genetikai
változás, virális hatás expresszió változás
-
szuppresszor gén inaktiváció
genetikai
változás, virális hatás(?) expresszió változás
-
epigenetikai háttér: DNS "hozzáférhetősége" - metiláció
imprinting
(jelentőség) expresszió változás
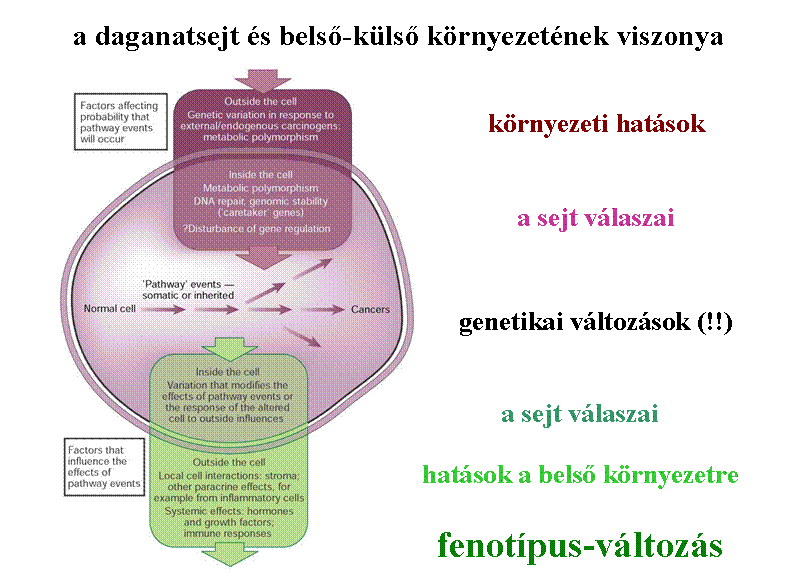
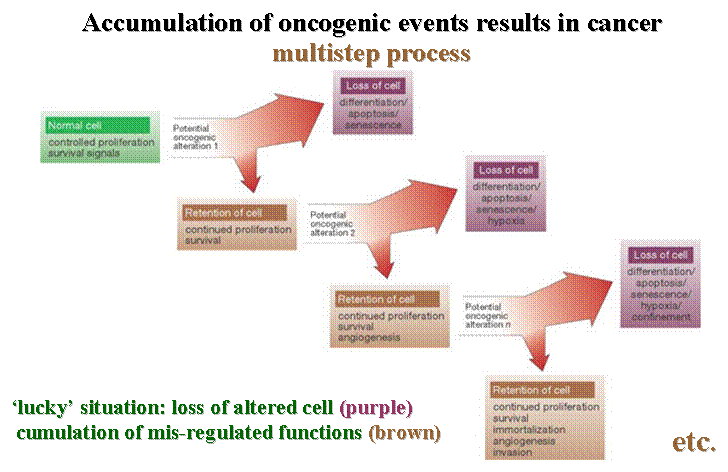
a daganat kialakulása
-
Knudson „Two hit” hypothesis- kétlépcsős modell
-
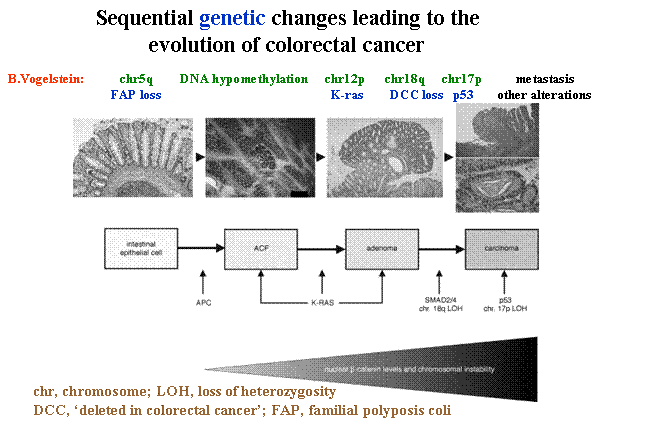
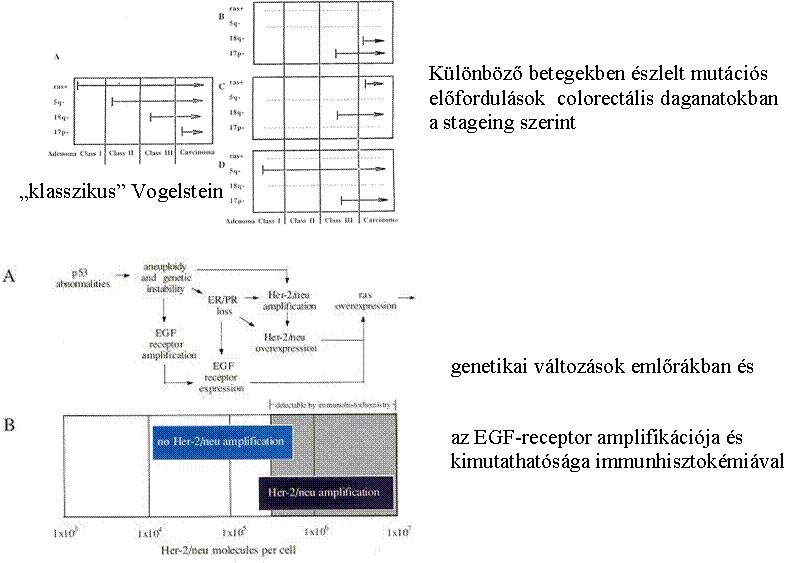
Bert Vogelstein soklépcsős folyamat
"iniciális esemény" – általában mutáció: proliferációs egyensúly megbomlása
familiáris daganatok: öröklött mutációk
progresszió -
hiperproliferatív
állapot
premalignus/malignus
sejtek
metasztatizáló sejtegyüttes
humán karcinogenezis modell:
megfigyelések, klinikai/pathologiai adatok alapján
|
|
|
|
|
|
|
|
|
|
|
|
|
|
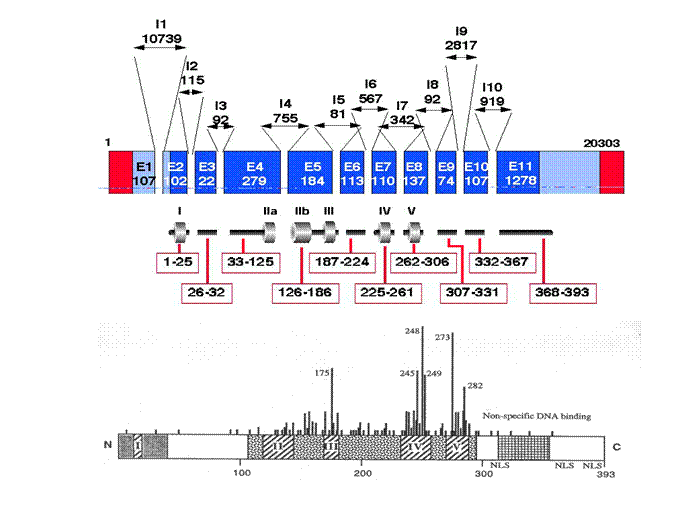
humán colorectális
minták analízise
Dukes' A: Invasion into but not through the bowel wall
Dukes' B: Invasion through the bowel wall penetrating the
muscle layer
but not involving lymph nodes
Dukes' C: Involvement of lymph nodes
Dukes' D: Widespread metastases
|
Dukes |
K-ras ex.1 |
P53 exon5 |
P53 exon6 |
P53 exon7 |
P53 exon8 |
Total |
|
A – 9 cases |
No
mutation |
No
mutation |
No
mutation |
No
mutation |
No
mutation |
0 (0%) |
|
B–43 cases |
9
cases |
5
cases |
2
cases |
6
cases |
2
cases |
24 (37%) |
|
C–11 cases |
6
cases |
5 cases |
2
cases |
9
cases |
3
cases |
25 (39%) |
|
D -
1 case |
1 case |
No
mutation |
No
mutation |
1 case |
1 case |
3 (5%) |
|
Total mutat, |
16 cases |
10 cases |
4 cases |
16 cases |
6 cases |
52 (81%) |
|
Sorszám, Dukes nem, kor |
K-ras exon1 |
P53 exon5 |
P53 exon6 |
P53 exon7 |
P53 exon8 |
|
53 (T1)
F 59 Dukes B centr. |
C8:
GTA~GTG C9:
GTT~GTA C10:
GGA~GTC C15:GGC~GGG |
C147:GTT~GAA |
Wt |
C253:
ACC~AAC |
C282:
CGG~CTC C283:CGC~CGG C288:
AAT~AAC C289:
CTC~CTA C291:
AAG~AAC C293:GGG~GCC C296:
CAC~CAG |
|
53 (T2)
F 59 Dukes B dist. |
Wt |
Wt |
Wt |
C249: AGG~GGG |
C281:GAC~G-C |
|
|
|
|
|
|
A daganatkeltő hatás kritériumai
Daganatkeltő: minden olyan ágens, ill. hatás,
amely:
• a kísérleti állatokban (ill. az emberben) daganatot okoz
vagy
• szignifikánsan emeli
az adott populációban létrejövő daganatok gyakoriságát
A daganat-kialakulás kockázatának becslése
•
Ismert
daganatkeltők listája: az ENSZ Nemzetközi Rákkutató Ügynöksége (IARC)
rendszeresen összeállítja, ill. felújítja a rendelkezésre álló kísérletes és
epidemiológiai adatok igen alapos kritikai elemzése alapján
•
Ennek
a listának a figyelembe vételével készülnek a nemzeti szabályozások, így a
hazai is (lásd a kémiai biztonságról 2000. évi XXV. törvény és végrehajtási
utasításainak vonatkozó mellékleteit)
•
A
primer daganat-prevenció egyik célja a hatékony kockázatkezeléssel a daganatok
gyakoriságának jelentős csökkentése.
|
|
a vegyi anyagok besorolása:
IARC
karcinogenitási kategóriák
• IARC 1: emberben
epidemiológiai adatokkal is bizonyítottan
daganatkeltő anyagok
• IARC 2A: Emberben valószínűleg daganatkeltő anyagok
(állatkísérletekben bizonyított hatás, de a humán epidemiológiai adatok még nem
elegendőek, vagy nem konkluzívak)
• IARC 2B: Emberben feltehetően daganatkeltő anyagok
(állatkísérletekben valószínű daganatkeltő hatás, humán epidemiológiai adatok
hiányoznak, vagy elégtelenek)
•
IARC 3.: Emberben daganatkeltés szempontjából nem
besorolható anyag
•
IARC 4.: nem rákkeltő
a karcinogének felismerésének korlátai
-
számos
ipari, mezőgazdasági és háztartási vegyi anyag igen
alacsony koncentrációban van jelen
-
az
élet során nagyszámú kémiai anyaggal exponálódunk
- hosszú 'lag fázissal' (az expozíciót követően hosszú idő után) jelentkeznek a daganatos
megbetegedések
figyelem!
'étkezési' karcinogenezis
valószínűsíthető összefüggéseket találtak egyes
daganatos megbetegedések
megjelenési
gyakorisága és a táplálkozási habitus között
néhány
asszociáció:
-
rost-szegény
diéta -- colon ca
-
zsíros
étrend -- emlő ca
-
bétel-levél
rágás -- szájüregi
ca
a daganat-terápia alapjai
rákellenes
hatóanyagok fejlesztése:
a daganatokban az
elmúlt bő évtized során azonosított molekuláris eltérések
figyelembevételével kell fejleszteni
a humán daganatsejtek szabályozási hibáit
egyre jobban ismerjük
daganatellenes szerek száma kicsiny:
alapvető nehézség:
- biztonságos és hatásos vegyületek
(alapmechanizmust kell gátolni…)
- nehezen tervezhető olyan kis molekula, amely a makromolekulák funkcióját
érzékenyen és egyúttal specifikusan befolyásolja
(pl. egy kis aktív centrum egy enzimen)
különösen nehéz
- a protein-protein
kölcsönhatások befolyásolása
(nagy felületen sok
kapcsolat)
- a defektív fehérjék funkciójának visszaállítása
(pl.
tumorszuppresszorok)
A hatásos daganaellenes vegyület:
szelektíven a daganatsejteket pusztítja el
szelektíven a daganatsejtek funkcióit függeszti fel
Több tucat vegyész, biokémikus és toxikológus
sokéves-sok-évtizedes munkája kell egy-egy effektív terápiás szer
kifejlesztéséhez, gyakorlatba kerüléséhez
A molekuláris genetika (és genomika) eredményeinek
alkalmazása hatóanyag-fejlesztésekben
mutációs modell:
a megváltozott
funciójú protein specifikus (kizárólagos) gátlása
siker!:
CML (Ph+) bcr-abl fúziós molekula, hiperaktív kináz
egyedi/eseti genetikai „screen” – a megváltozott tulajdonságok (mRNS, fehérjék)
a daganatos betegségben („cDNA chip”)
|
|
|
|
|
|
!! mutagén hatások – másodlagos daganat indukció !!
sok
évvel később jelenik meg
nem
rokon a primer, ’ellátott’ daganattal
|
|
a daganatsejt fiziológiai (endokrin,
receptor) működése
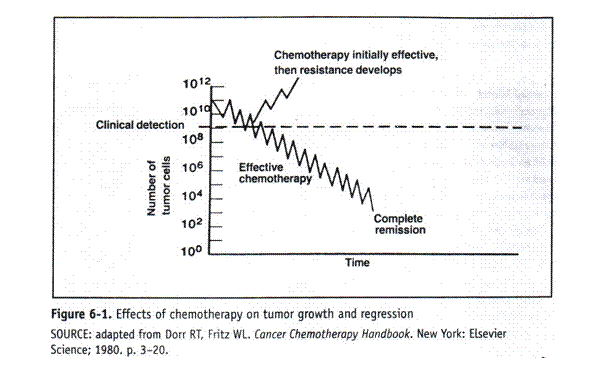
a kemoterápia hatása a daganatnövekedésre és regresszióra
|
|
|
|
|
|
|
|
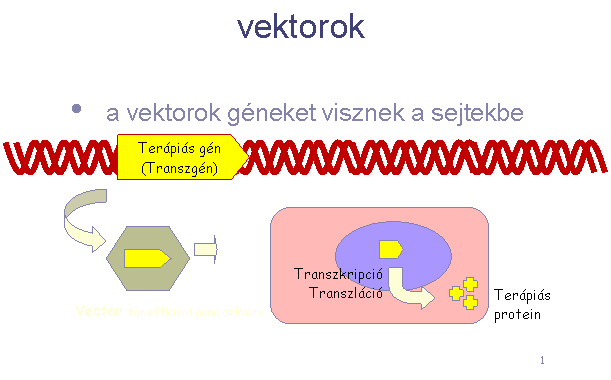
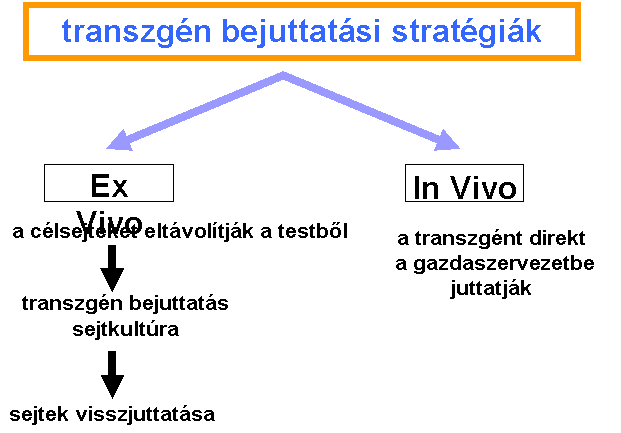
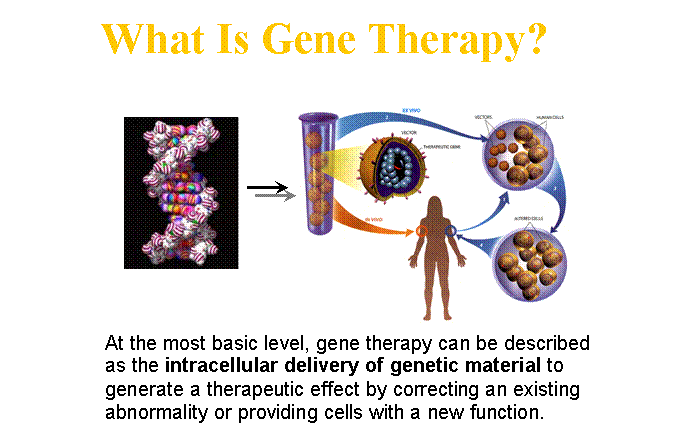
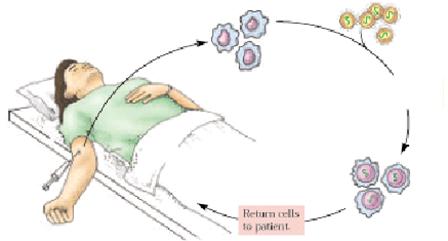
daganatellenes
hatás direkt bejuttatása:
génterápia
(’targeting’)
vektor -- gén
|
|
|
|
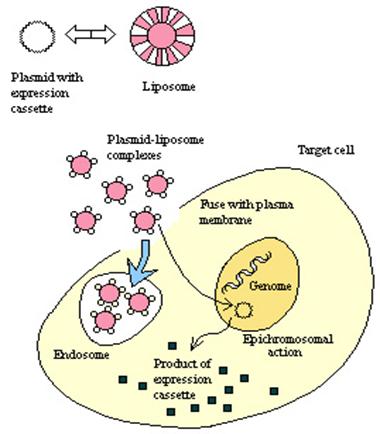
nem-virális génátvitel:
liposzómában
|
|
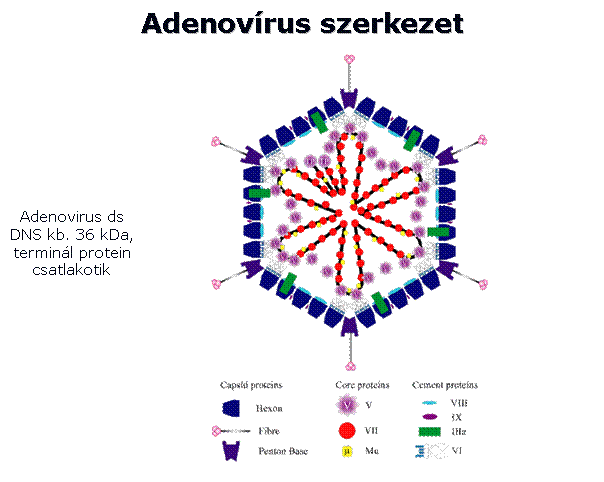
virális génátvitel
|
|
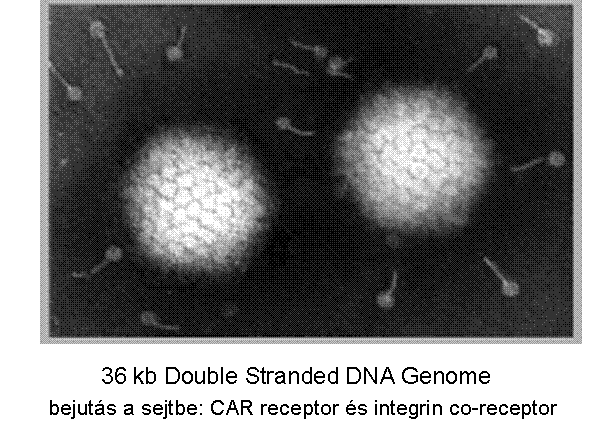
Adenovírus EM
|
|
|
|
alkalmazási mód (?)
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
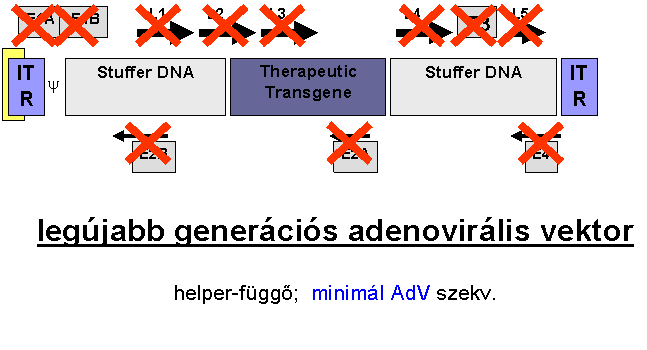
AAV - adeno-asszociált vírus - kísérleti expressziós rendszer
. . . és ki tudja, mit hoz a jövő . . .
kutatás
egyedi terápia
. . .
|
|
|
|
|
|
|
|
|
|